【資料No.1】2.5_臨床に関する概括資料 (150 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29325.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会(令和4年度第5回 11/22)、医薬品第二部会(令和4年度第13回 11/22)(合同開催)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
2.5 臨床に関する概括評価
S-217622
125 mg
N = 407
S-217622
250 mg
N = 398
Placebo
N = 402
Stratified log-rank test vs. placebo [b]
- One-sided p-value
- Two-sided p-value
0.0297
0.0594
0.0016
0.0031
-----
Stratified Peto-Prentice's generalized Wilcoxon test
vs. placebo [b]
- One-sided p-value
- Two-sided p-value
0.0060
0.0120
0.0017
0.0035
-----
Stratified Cox proportional hazard model [b]
- Hazard ratio [95% CI]
1.17 [0.99, 1.38]
1.27 [1.08, 1.50]
--- Two-sided p-value
0.0582
0.0040
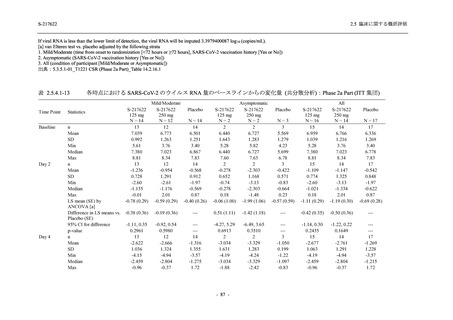
--Merged Efficacy Analysis Population is defined as a merged population of Intention-to-Treat Population in Phase 2a Part,
Phase 3 Part, and Phase 2b/3 Part and Intention-to-Treat 1 Population in Phase 2b Part.
CI = Confidence Interval; Min = Minimum; Max = Maximum
5 symptoms (stuffy or runny nose, sore throat, cough, feeling hot or feverish, and low energy or tiredness)
[a] +: Max includes censored data.
[b] Adjusted by the following stratum (SARS-CoV-2 vaccination history [Yes or No])
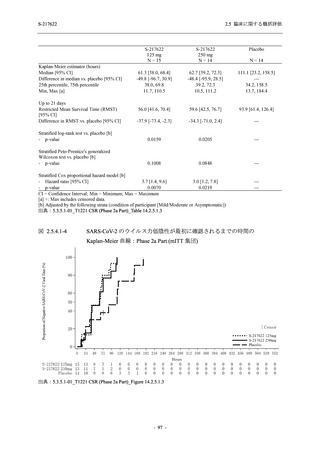
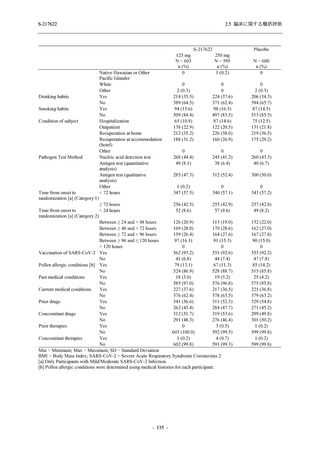
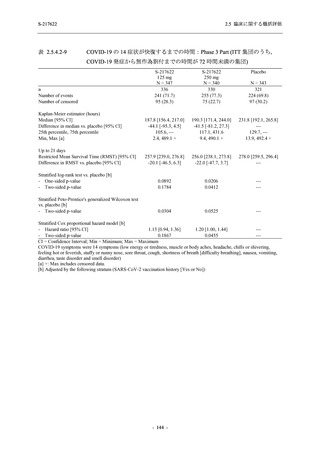
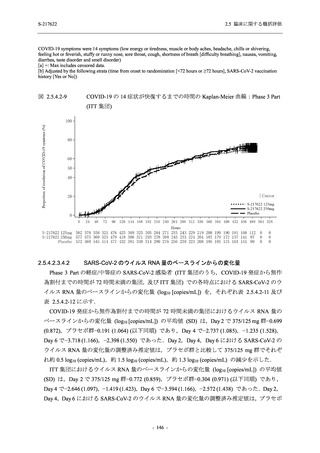
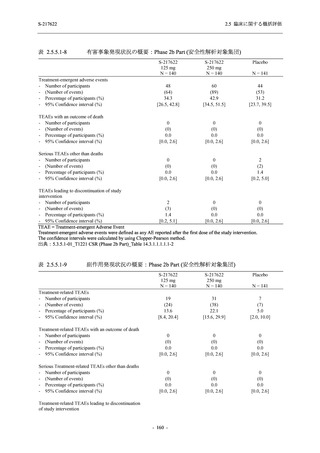
図 2.5.4.2-10
COVID-19 の 5 症状が快復するまでの時間の Kaplan-Meier 曲線:Phase 2a
Part,Phase 2b Part,Phase 3 Part 併合 (ITT 集団のうち,COVID-19 発症から
無作為割付までの時間が 72 時間未満の集団)
2.5.4.2.3.6
部分集団における有効性
Phase 3 Part の主要評価項目である COVID-19 の 5 症状が快復するまでの時間について,軽症
/中等症の SARS-CoV-2 感染者 (ITT 集団のうち,COVID-19 発症から無作為割付までの時間が
72 時間未満の集団) を対象に,SARS-CoV-2 ワクチン接種及び花粉症の有無別の部分集団解析
を実施した.Phase 3 Part の実施時期が花粉症の時期と重なっており,花粉症の症状が評価対象
- 150 -