【資料No.1】2.5_臨床に関する概括資料 (198 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29325.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会(令和4年度第5回 11/22)、医薬品第二部会(令和4年度第13回 11/22)(合同開催)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
2.5 臨床に関する概括評価
活動の制限等が社会的な問題となっていることから,自宅等でも簡便に使用可能で,重症化リ
スク因子の有無やワクチン接種の有無にかかわらず使用可能である経口の抗ウイルス薬に対す
る社会的ニーズが高まっている (2.5.1.2.2 項参照).
2.5.6.2
2.5.6.2.1
ベネフィット
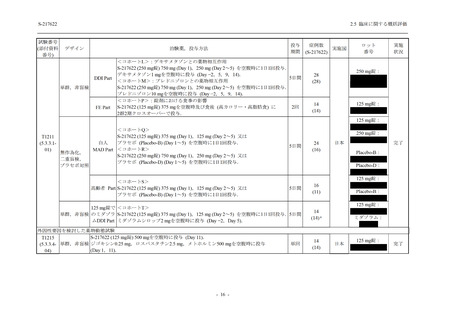
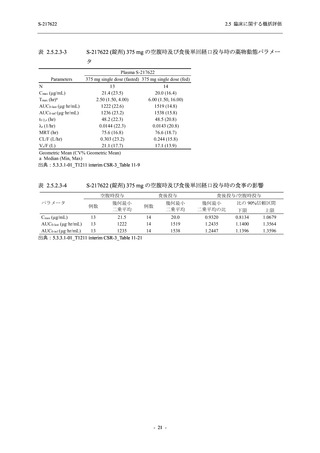
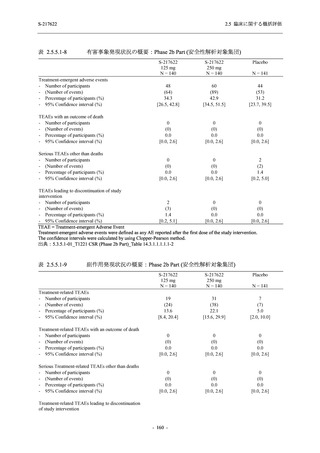
ウイルス力価及びウイルス RNA 量に基づく,抗ウイルス効果が示された
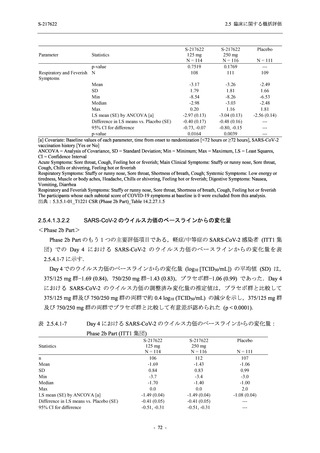
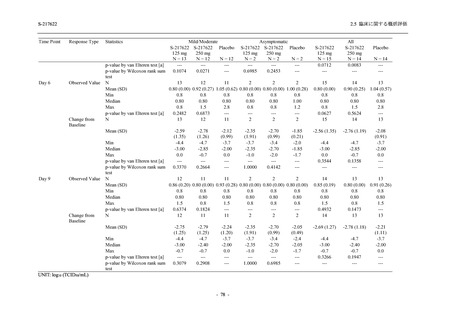
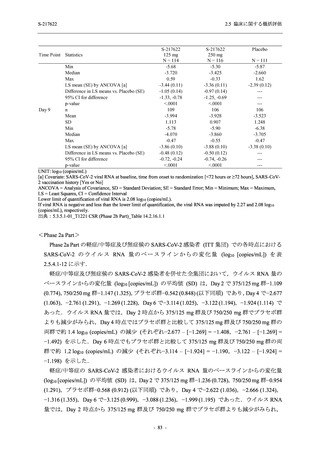
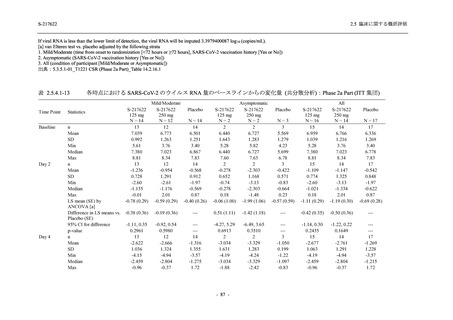
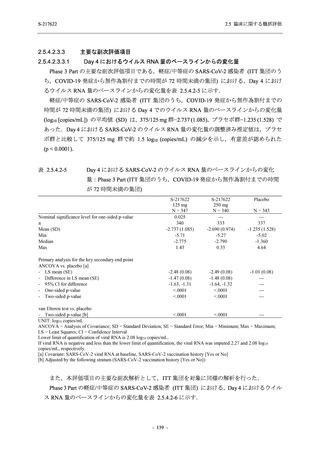
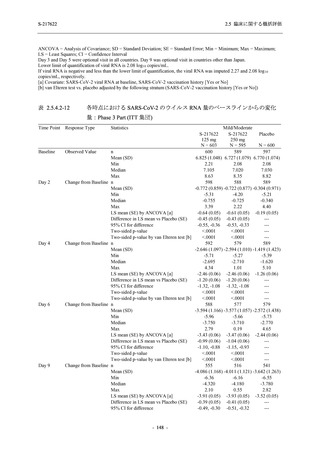
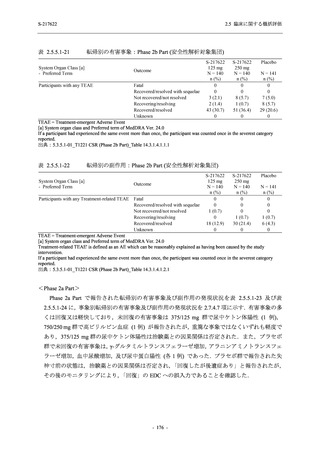
T1221 試験 Phase 2b Part において,Day 4 における SARS-CoV-2 のウイルス力価のベースライ
ンからの調整済み変化量の推定値は,プラセボ群と比較して 375/125 mg 群及び 750/250 mg 群
の両群で約 0.4 log10 (TCID50/mL) の減少を示し,375/125 mg 群及び 750/250 mg 群の両群でプラ
セボ群と比較して有意差が認められた (p < 0.0001).Day 2 及び Day 6 においても,375/125 mg
群及び 750/250 mg 群の両群で有意差が認められた (Day 2:それぞれ p <0.0001,p <0.0001,
Day 6:
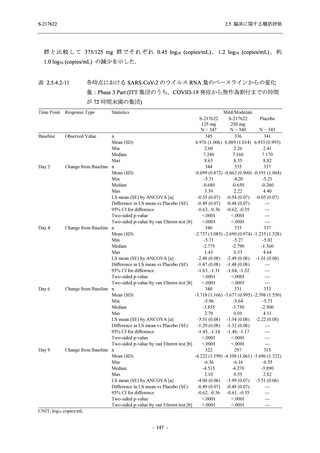
それぞれ p = 0.0012,p = 0.0010).また,Day 2,Day 4,Day 6 における SARS-CoV-2 のウイルス
RNA 量の調整済み変化量の推定値は,プラセボ群と比較して 375/125 mg 群及び 750/250 mg 群
の両群でそれぞれ約 0.4 log10 (copies/mL),約 1.2 log10 (copies/mL),約 1.0 log10 (copies/mL) の減
少を示し,いずれの時点においても 375/125 mg 群及び 750/250 mg 群の両群でプラセボ群と比
較して有意差が認められた (いずれも p < 0.0001).
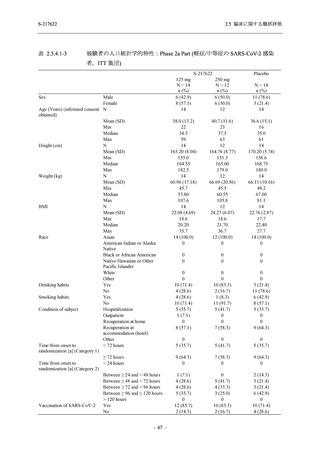
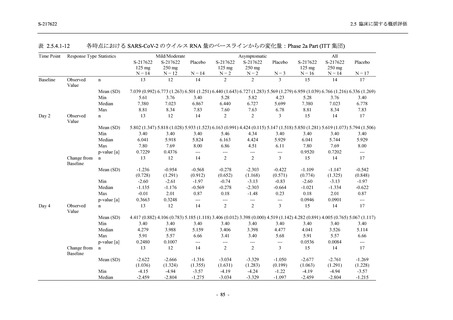
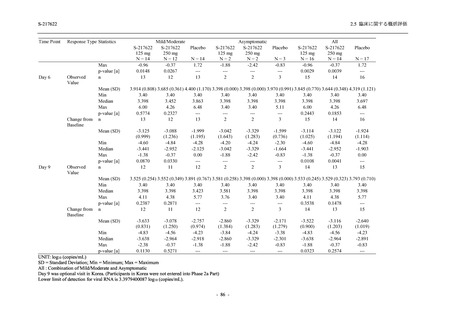
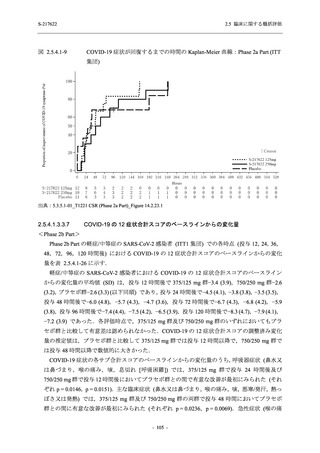
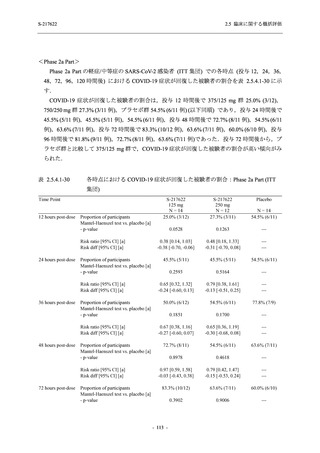
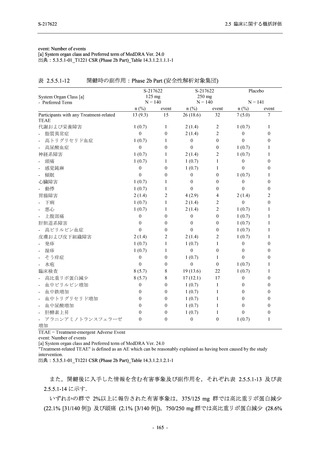
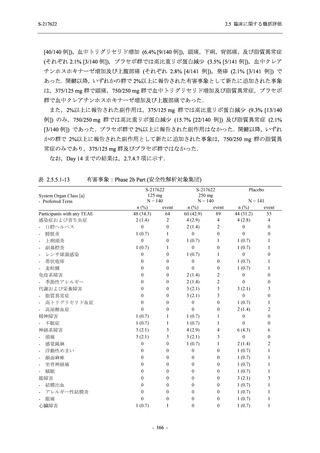
T1221 試験 Phase 2a Part において,軽症/中等症及び無症候の SARS-CoV-2 感染者を併せた全
集団で,ウイルス力価のベースラインからの変化量は,Day 4 時点でプラセボ群と比較して約
1 log10 (TCID50/mL) の減少を示し,調整済み変化量の推定値もプラセボ群と比較して約 1 log10
(TCID50/mL) の減少を示した (2.5.4.1.3.2.2 項参照).ウイルス RNA 量のベースラインからの変
化量も,Day 4 時点でプラセボ群と比較して約 1.4 log10 (copies/mL) の減少を示し,調整済み変
化量の推定値もプラセボ群と比較して約 1 log10 (copies/mL) の減少を示した (2.5.4.1.3.3.1 項参
照).また,ウイルス学的検査に基づくその他複数の評価項目においても,抗ウイルス効果が期
待される結果が得られた (2.5.4.1.3.3.2~2.5.4.1.3.3.5 項参照).
抗ウイルス薬による薬物治療は SARS-CoV-2 の感染後早期に開始し,ウイルス増殖を速やか
に抑制し,ウイルス感染に起因する過剰な炎症や免疫反応を抑えることが症状改善に有益と考
えられている.上記の結果から,本剤投与による抗ウイルス効果が確認されたため,本剤は
SARS-CoV-2 に対する抗ウイルス薬として新たな治療選択肢となり得ると考える.
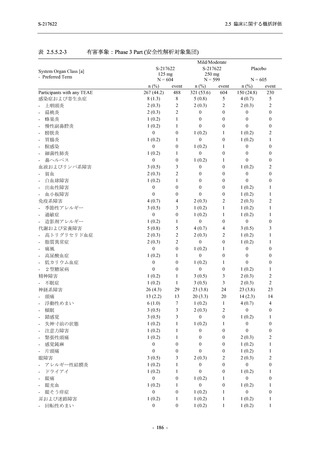
T1221 試験 Phase 3 Part の結果に基づき,再検討した内容を追記する.
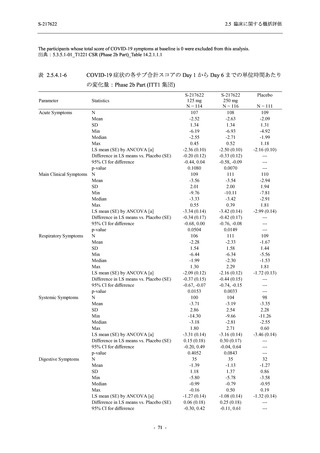
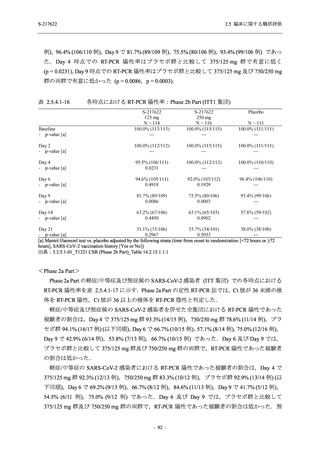
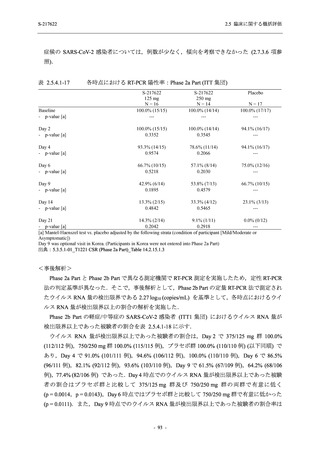
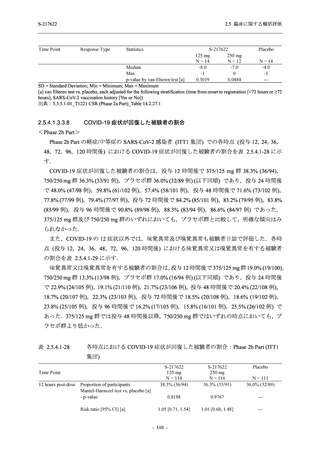
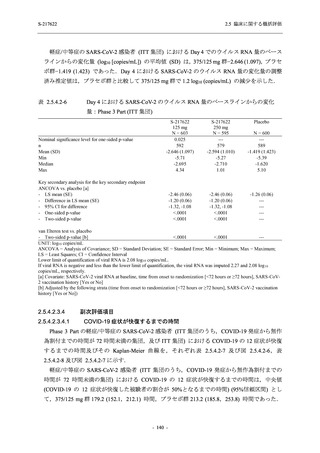
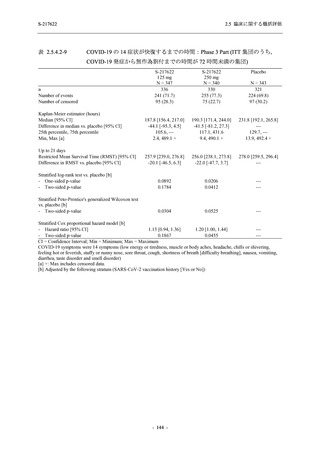
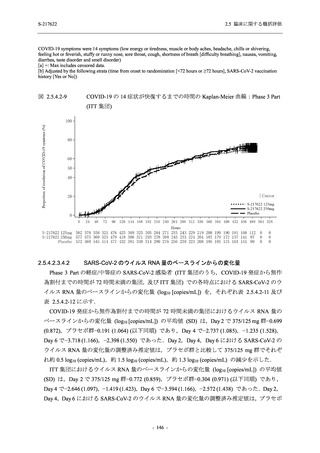
T1221 試験 Phase 3 Part の主要な副次評価項目である,ITT 集団のうち,COVID-19 発症から
無作為割付までの時間が 72 時間未満の集団における Day 4 でのウイルス RNA 量のベースライ
ンからの変化量について,その調整済み推定値は,プラセボ群と比較して 375/125 mg 群で約
1.5 log10 (copies/mL) の減少を示し,統計学的に有意な差が認められたことから (p < 0.0001),ウ
イルス RNA 量を基準とした抗ウイルス効果が検証された.ITT 集団でも,ウイルス RNA 量の
減少が認められた (2.5.4.2.3.3.1 項参照).
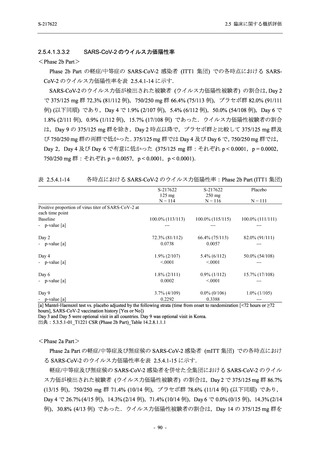
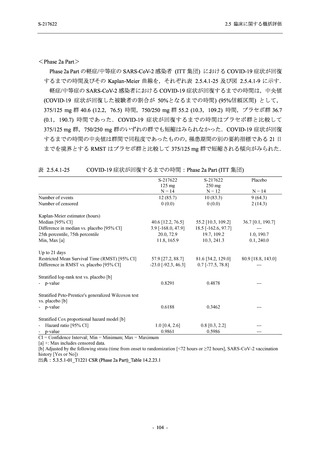
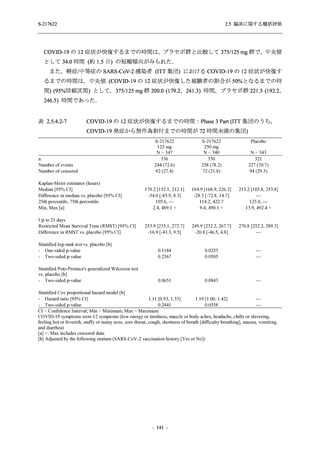
もう一つの主要な副次評価項目である SARS-CoV-2 のウイルス力価陰性が最初に確認される
までの時間については,現時点では結果が得られていない.しかし,Phase 2a Part 及び Phase 2b
- 198 -