【資料No.1】2.5_臨床に関する概括資料 (49 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29325.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会(令和4年度第5回 11/22)、医薬品第二部会(令和4年度第13回 11/22)(合同開催)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
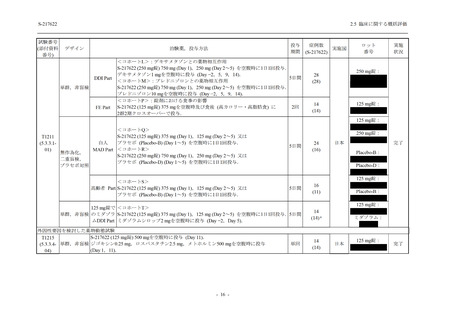
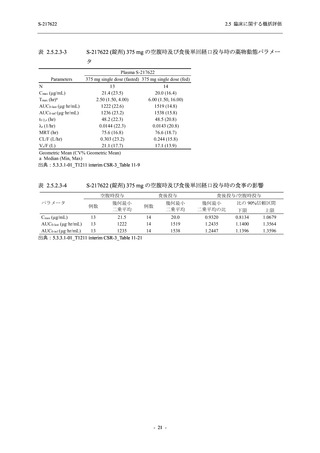
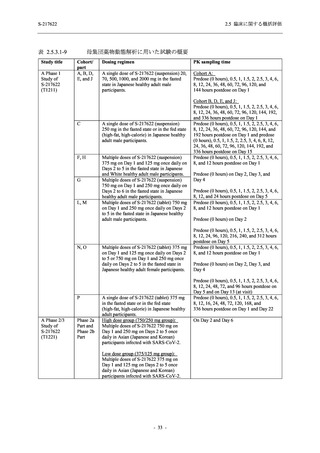
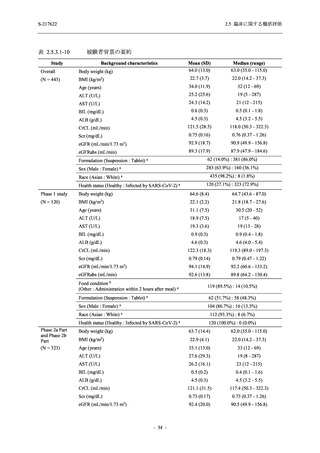
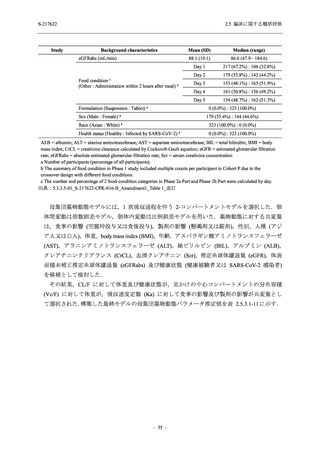
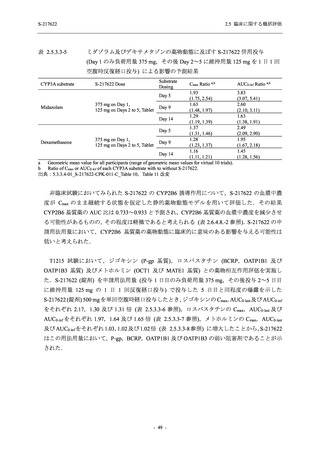
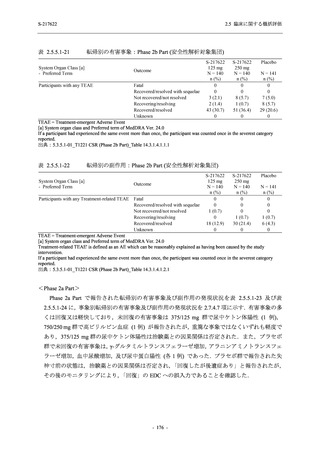
表 2.5.3.3-5
2.5 臨床に関する概括評価
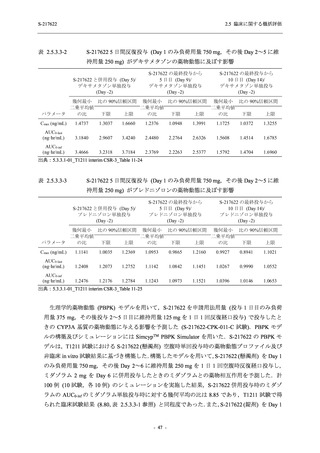
ミダゾラム及びデキサメタゾンの薬物動態に及ぼす S-217622 併用投与
(Day 1 のみ負荷用量 375 mg,その後 Day 2~5 に維持用量 125 mg を 1 日 1 回
空腹時反復経口投与) による影響の予測結果
CYP3A substrate
S-217622 Dose
Substrate
Dosing
Cmax Ratio a,b
1.93
(1.75, 2.54)
1.63
375 mg on Day 1,
Midazolam
Day 9
125 mg on Days 2 to 5, Tablet
(1.48, 1.97)
1.29
Day 14
(1.19, 1.39)
1.37
Day 5
(1.31, 1.46)
1.28
375 mg on Day 1,
Dexamethasone
Day 9
125 mg on Days 2 to 5, Tablet
(1.23, 1.37)
1.16
Day 14
(1.11, 1.21)
a
Geometric mean value for all participants (range of geometric mean values for virtual 10 trials).
b
Ratio of Cmax or AUC0-inf of each CYP3A substrate with to without S-217622.
出典:5.3.3.4-01_S-217622-CPK-011-C_Table 10,Table 11 改変
Day 5
AUC0-inf Ratio a,b
3.83
(3.07, 5.41)
2.60
(2.10, 3.11)
1.63
(1.38, 1.91)
2.49
(2.09, 2.90)
1.95
(1.67, 2.18)
1.45
(1.28, 1.56)
非臨床試験においてみられた S-217622 の CYP2B6 誘導作用について,S-217622 の血漿中濃
度が Cmax のまま継続する状態を仮定した静的薬物動態モデルを用いて評価した.その結果
CYP2B6 基質薬の AUC 比は 0.733~0.933 と予測され,CYP2B6 基質薬の血漿中濃度を減少させ
る可能性があるものの,その程度は軽微であると考えられる (表 2.6.4.8.-2 参照).S-217622 の申
請用法用量において,CYP2B6 基質薬の薬物動態に臨床的に意味のある影響を与える可能性は
低いと考えられた.
T1215 試験において,ジゴキシン (P-gp 基質),ロスバスタチン (BCRP,OATP1B1 及び
OATP1B3 基質) 及びメトホルミン (OCT1 及び MATE1 基質) との薬物相互作用評価を実施し
た.S-217622 (錠剤) を申請用法用量 (投与 1 日目のみ負荷用量 375 mg,その後投与 2~5 日目
に維持用量 125 mg の 1 日 1 回反復経口投与) で投与した 5 日目と同程度の曝露を示した
S-217622 (錠剤) 500 mg を単回空腹時経口投与したとき,
ジゴキシンの Cmax,
AUC0-last 及び AUC0-inf
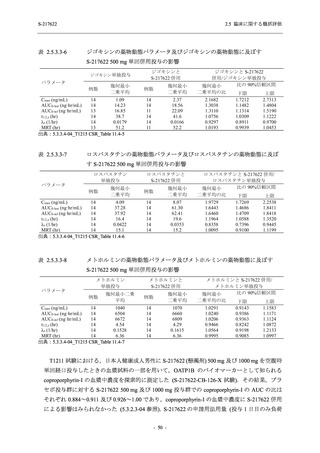
をそれぞれ 2.17,1.30 及び 1.31 倍 (表 2.5.3.3-6 参照),ロスバスタチンの Cmax,AUC0-last 及び
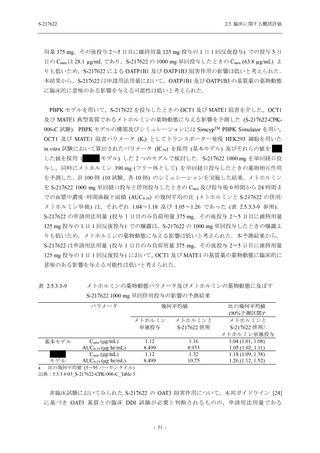
AUC0-inf をそれぞれ 1.97,1.64 及び 1.65 倍 (表 2.5.3.3-7 参照),メトホルミンの Cmax,AUC0-last
及び AUC0-inf をそれぞれ 1.03,
1.02 及び 1.02 倍 (表 2.5.3.3-8 参照) に増大したことから,
S-217622
はこの用法用量において,P-gp,BCRP,OATP1B1 及び OATP1B3 の弱い阻害剤であることが示
された.
- 49 -