提案書04(0599頁~0801頁)医療技術評価・再評価提案書 (154 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000190899_00011.html |
| 出典情報 | 中央社会保険医療協議会 診療報酬調査専門組織・医療技術評価分科会(令和5年度第1回 11/20)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
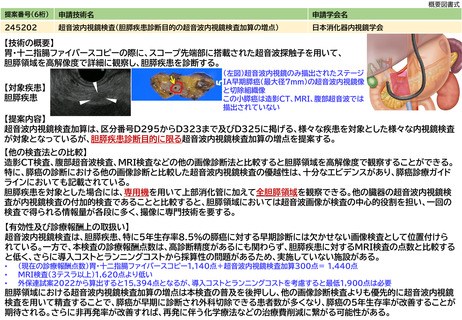
標準治療がない固形がん患者又は局所進行若しくは転移が認められ標準治療が終了となった固形がん患者(終了が見込まれる者を含む。)であっ
て、関連学会の化学療法に 関するガイドライン等に基づき、全身状態及び臓器機能等から、当該検査施行後に化学療法の適応となる可能性が高
いと主治医が判断した者に対して実施する場合に限り算定できる。3学会(日本臨床腫瘍学会、日本癌学会、日本癌治療学会)合同ガイダンスで
は、小児がんは標準治療が確立していないものが多いことなどから、遺伝子パネル検査の実施を考慮する対象となっている。
②現在の診療報酬上の取扱い
・対象とする患者
・医療技術の内容
・点数や算定の留意事項
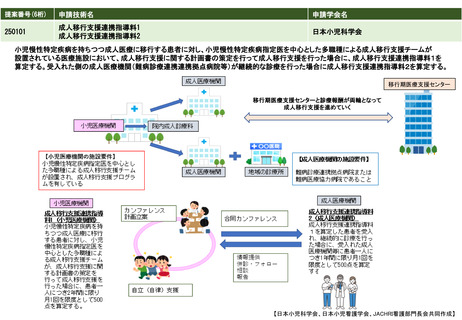
・医療技術の内容:
固形腫瘍の腫瘍細胞を検体とし、100以上のがん関連遺伝子の変異等を検出するがんゲノムプロファイリング検査に用いる医療機器等として薬事
承認又は認証を得ているシークエンサーシステムを用いて、包括的なゲノムプロファイルの取得を行う。結果をがんゲノム医療中核拠点病院(ま
たはがんゲノム医療拠点病院)にて整備したエキスパートパネルを介してレポート作成し、返却する。
・点数や算定の留意事項:
(1) 「1」検体提出時については、固形腫瘍の腫瘍細胞を検体とし、100 以上のがん関連遺伝子の変異等を検出するがんゲノムプロファイリン
グ検査に用いる医療機器等として薬事承認又は認証を得ている次世代シーケンシングを用いて、包括的なゲノムプロファイルの取得を行う場合
に、患者1人につき1回に限り算定できる。
(2) 「2」結果説明時については、「1」検体提出時で得た包括的なゲノムプロファイル の結果について、当該検査結果を医学的に解釈するた
めの多職種(がん薬物療法に関する専門的な知識及び技能を有する医師、遺伝医学に関する専門的な知識及び技能を有する医師、遺伝カウンセリ
ング技術を有する者等)による検討会(エキスパートパネル) での検討を経た上で患者に提供し、治療方針等について文書を用いて患者に説明
する場合に、患者1人につき1回に限り算定できる。
D
診療報酬区分(再掲)
診療報酬番号(再掲)
D006-19
医療技術名
がんゲノムプロファイリング検査
小児がん患者に対してゲノムプロファイリング検査を実施することで、20-24%の患者が何らかの治療標的となる遺伝子変異を検出したと報告され
ている。標準治療の確立していないがん患者に対する治療選択を広げることにつながる。
治癒率、死亡率やQOLの改善等の長期予 また、臨床研究JCCG-TOP2において、がんゲノムプロファイリング検査(新Todai OncoPanel)を研究費により実施する枠組みを提供したところ、
後等のアウトカム
2022年1月~2023年2月の13か月で200名の患者が登録し、がんゲノムプロファイリング検査を受け、そのうち75%で診療に有用なゲノム異常が確認
③再評価の根
拠・有効性
された
ガイドライン等での位置づけ
④普及性の変化
※下記のように推定した根拠
年間対象者数の
変化
年間実施回数の
変化等
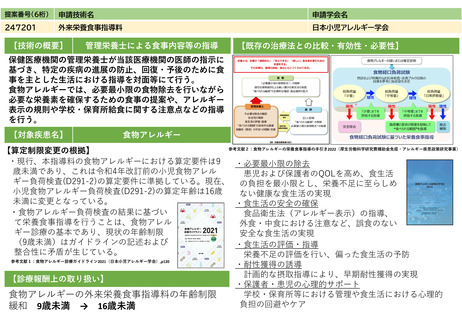
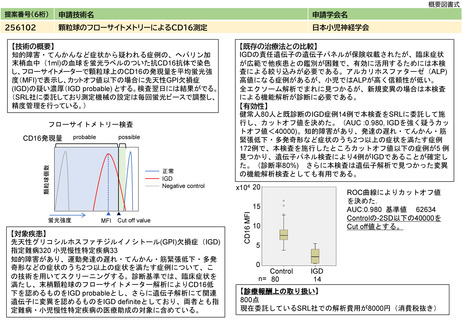
日本小児血液・がん学会の実態調査により83施設から回答を得た結果によると、2019年6月以降に出検されたがんゲノムプロファイリング検査は
779件(およそ4年間のため、年間194件)であったのに対し、「入院中に算定できないため検査ができなかった」症例が15例であり、入院中の出
検が算定できるようになった場合、これらが出検されることで年間4件程度が新たに検査として実施されると推測される。(検査は一人1回に限定
されている)
見直し前の症例数(人)
194
見直し後の症例数(人)
198
見直し前の回数(回)
194
見直し後の回数(回)
198
⑤医療技術の成熟度
・学会等における位置づけ
・難易度(専門性等)
・施設基準
(技術の専門性
等を踏まえ、必
要と考えられる
要件を、項目毎
に記載するこ
と)
3学会(日本臨床腫瘍学会、日本癌学会、日本癌治療学会)合同ガイダンスでは、小児がん
ガイドライン等での記載あり(右欄に詳細を記載す
は標準治療が確立していないものが多いことなどから、診断時を含めて遺伝子パネル検査
る。)
の実施を考慮する対象となっている。
3学会(日本臨床腫瘍学会、日本癌学会、日本癌治療学会)合同ガイダンスでは、小児がんは標準治療が確立していないものが多いことなどか
ら、診断時を含めて遺伝子パネル検査の実施を考慮する対象となっている。
施設の要件
(標榜科、手術件数、検査や手術の体 がんゲノム医療中核拠点病院・がんゲノム医療拠点病院・がんゲノム医療連携病院に指定されている施設から検査を提出することができる。
制等)
人的配置の要件
(医師、看護師等の職種や人数、専門 上記の施設要件を満たすための医師・病理医・遺伝カウンセラーが必要である。
性や経験年数等)
その他
(遵守すべきガイドライン等その他の なし
要件)
⑥安全性
・副作用等のリスクの内容と頻度
該当しない
⑦倫理性・社会的妥当性
(問題点があれば必ず記載)
問題なし
⑧点数等見直し
の場合
見直し前
該当なし
見直し後
該当なし
その根拠
該当なし
752