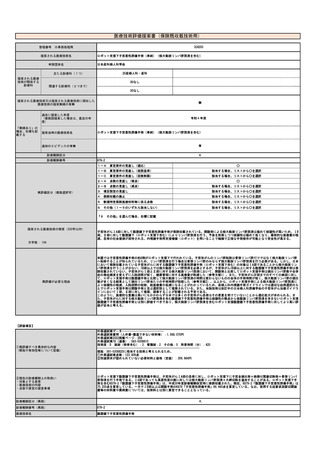
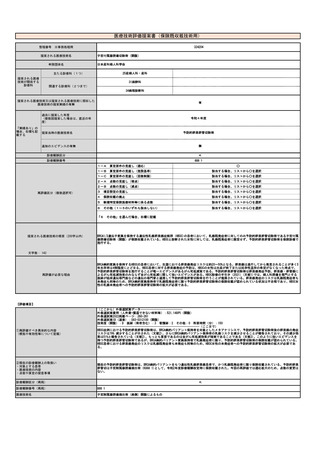
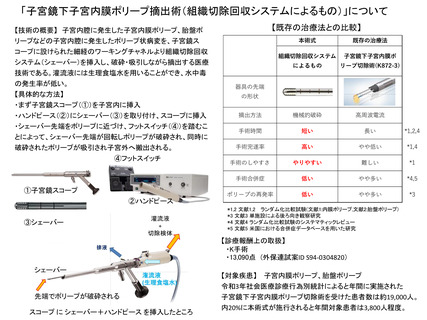
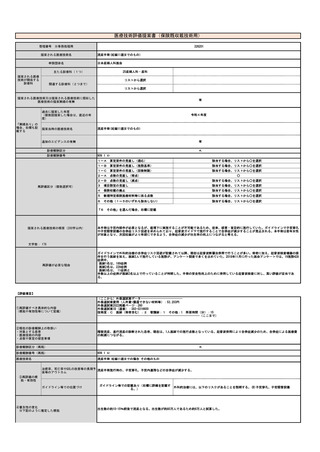
提案書10(1802頁~2002頁)医療技術評価・再評価提案書 (180 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000190899_00011.html |
| 出典情報 | 中央社会保険医療協議会 診療報酬調査専門組織・医療技術評価分科会(令和5年度第1回 11/20)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
整理番号
提案される医療技術名
申請団体名
330203
鏡視下咽頭悪性腫瘍手術(軟口蓋悪性腫瘍手術を含む。)(内視鏡手術用支援機器を用いる場合)、鏡視下喉頭悪性腫瘍手術(内視鏡手術
用支援機器を用いる場合)
日本耳鼻咽喉科・頭頸部外科学会
※ 薬事承認されていない医薬品、医療機器又は体外診断薬を使用した技術は、原則として医療技術評価分科会での評価の対象外である。承認見込みの場合、令和5年(2023年)8
月末日迄に承認取得が可能な場合のみ、評価の対象となることに留意すること。
※
医薬品、医療機器又は体外診断薬については、当該技術の核となるものについて必ず具体的な薬品名、製品名を記載すること。
※
該当する製品の添付文書を添付すること。
※
薬事承認上の内容等が不明な場合は、添付文書を確認するか、製造販売会社等に問い合わせること。
※
記載が不十分であると判断した場合は評価の対象外となるため、必要事項をもれなく記載すること。
【医薬品について】
名称(販売名、一般名、
製造販売企業名)
薬事承認番号
収載年月日
薬事承認上の
「効能又は効果」
薬事承認番号
収載年月日
薬事承認上の
「使用目的、効能又は効果」
薬価(円)
備考
※薬事申請及び公知申請の状況等(薬
事承認見込みの場合等はその旨を記
載)
特になし
【医療機器について】
名称(販売名、一般名、
製造販売企業名)
da Vinci Siサージカルシステム
da Vinci Xiサージカルシステム
da Vinci X サージカルシステム
da Vinci Sp サージカルシステム
22400BZX0038700
2018/12/21
0
本品は、一般消化器外科、胸部外科、心臓
外科(心停止下で心内操作を行う手術に限
る。)、泌尿器科、婦人科及び頭頸部外科
(経口的に行う手術に限る。)の各領域に
おいて内視鏡手術を実施する際に、組織又
は異物の把持、切開、鈍的/鋭的剥離、近
置、結紮、高周波電流を用いた切開・凝
固、縫合及び操作、並びに手術付属品の挿
入・運搬を行うために、術者の内視鏡手術
器具操作を支援する装置である。
22700BZX0011200
2018/12/21
0
本品は、一般消化器外科、胸部外科、心臓
外科(心停止下で心内操作を行う手術に限
る。)、泌尿器科 、 婦人科 及び頭頸部外
科(経口的に
行う手術に限る。)の各領域において内視
鏡手術を実施する際に、組織又は異物の把
持、切開、鈍的/鋭的剥離、近置 、結紮、
高周波電流を用いた切開・凝固、縫合及び
操作、並びに手術付属品の挿入・運搬を行
うために、術者の内視鏡手術器具操作を支
援する装置である。
23000BZX0009000
2019/12/25
0
本品は、一般消化器外科、胸部外科、心臓
外科(心停止下で心内操作を行う手術に限
る。)、泌尿器科 、婦人科 及び頭頸部外
科(経口的に行う手術に限る。)の各領域
において内視鏡手術を実施する際に、組織
又は異物の把持、切開、鈍的/鋭的剥離、近
置結紮、高周波電流を用いた切開・凝固、
縫合及び操作、並びに手術付属品の挿入・
運搬を行うために、術者の内視鏡手術器具
操作を支援する装置である。
30400BZX0022000
2022/09
0
本品は、一般消化器外科、胸部外科(心臓
外科並びに肋間からのアプローチ手術を除
く。)、泌尿器科、婦人科及び頭頸部外科
(経口的に行う手術に限る。)の各領域にお
いて内視鏡手術を実施する際に、組織又は
異物の把持、切開、鈍的/鋭的剥離、近置、
結紮、高周波電流を用いた切開・凝固、縫
合及び操作、並びに手術付属品の挿入・運
搬を行うために、術者の内視鏡手術器具操
作を支援する装置である。
特定保険医療材料に該当する場合は、
番号、名称、価格を記載
特定保険医療材
(※薬事申請及び公知申請の状況等(薬
料
事承認見込みの場合等はその旨を記
載)
【体外診断用医薬品(検査用試薬)について】
名称(販売名、一般名、
製造販売企業名)
薬事承認番号
収載年月日
薬事承認上の「使用目的」
特になし
【その他記載欄(上記の欄に記載しきれない内容がある場合又は再生医療等製品を使用する場合には以下を記入すること)】
特になし
1981
備考
※薬事申請及び公知申請の状況等(薬事承認見込みの場
合等はその旨を記載)