提案書01(0001頁~0202頁)医療技術評価・再評価提案書 (166 ページ)
出典
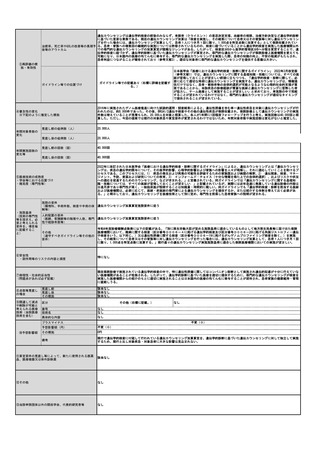
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000190899_00011.html |
| 出典情報 | 中央社会保険医療協議会 診療報酬調査専門組織・医療技術評価分科会(令和5年度第1回 11/20)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
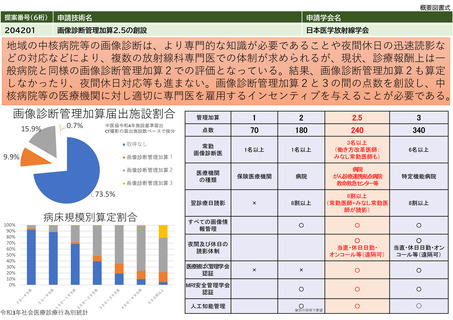
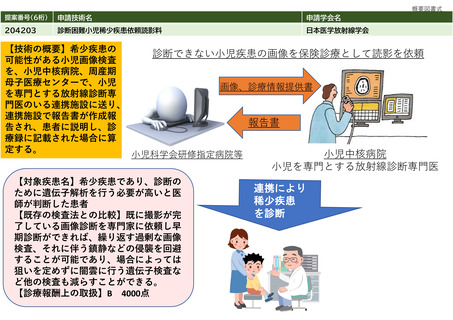
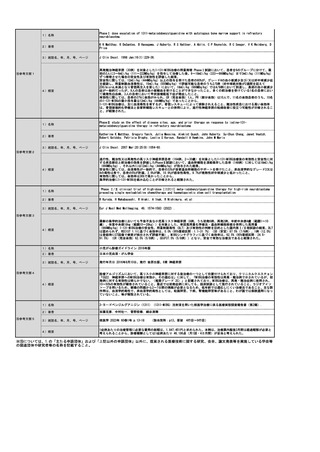
提案番号(6桁)
申請技術名
申請学会名
214201
クロストリジオイデス・ディフィシルのトキシンB遺伝子検出
日本化学療法学会
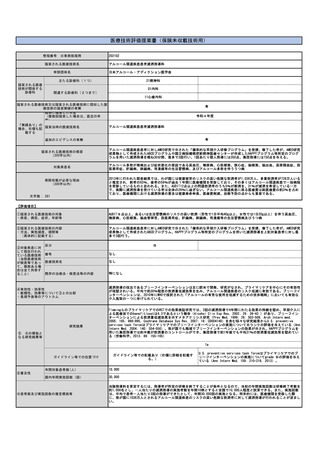
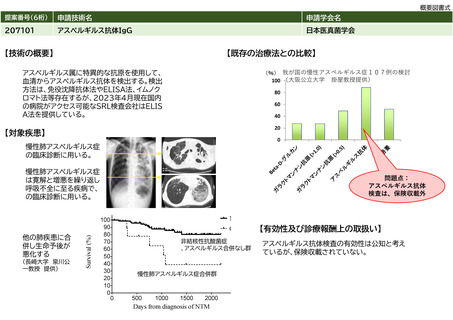
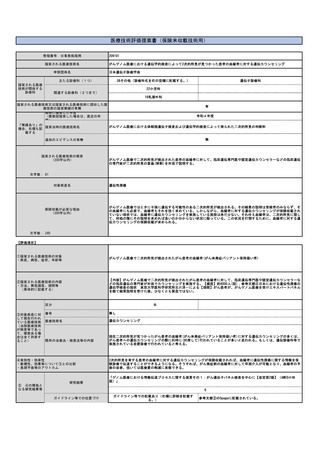
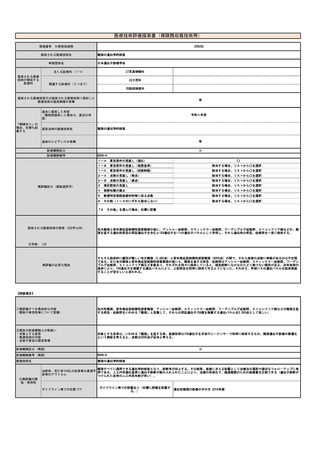
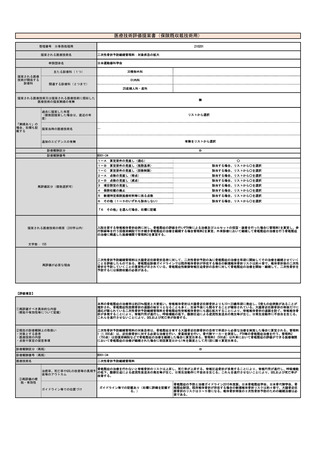
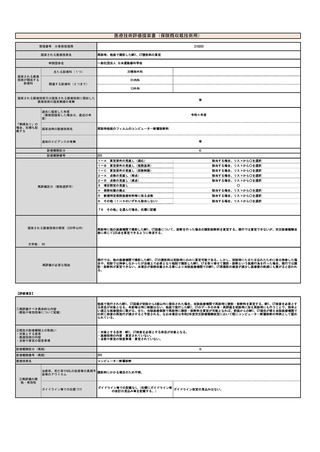
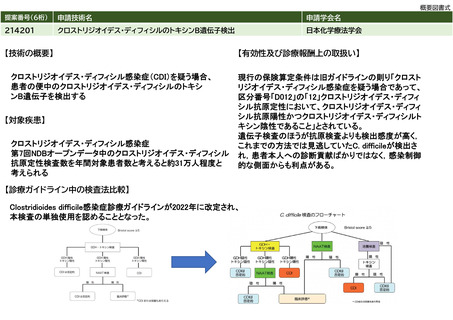
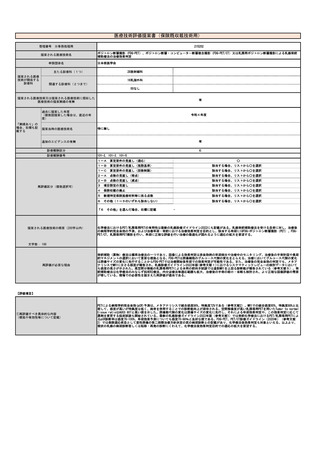
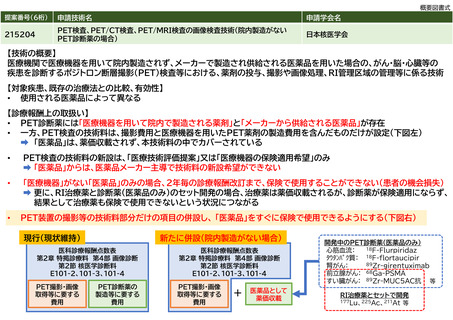
【技術の概要】
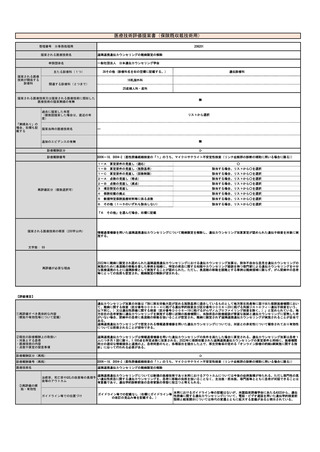
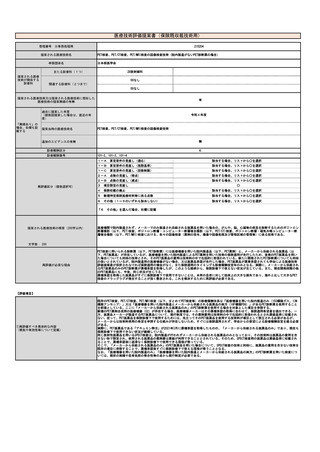
【有効性及び診療報酬上の取扱い】
クロストリジオイデス・ディフィシル感染症(CDI)を疑う場合、
患者の便中のクロストリジオイデス・ディフィシルのトキシ
ンB遺伝子を検出する
【対象疾患】
クロストリジオイデス・ディフィシル感染症
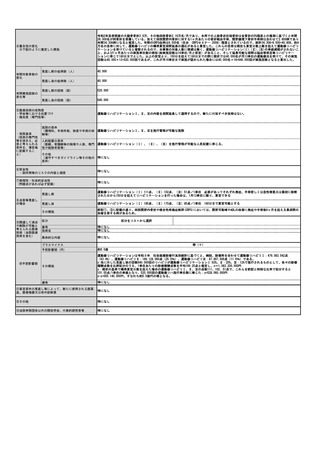
第7回NDBオープンデータ中のクロストリジオイデス・ディフィシル
抗原定性検査数を年間対象患者数と考えると約31万人程度と
考えられる
現行の保険算定条件は旧ガイドラインの則り「クロスト
リジオイデス・ディフィシル感染症を疑う場合であって、
区分番号「D012」の「12」クロストリジオイデス・ディフィ
シル抗原定性において、クロストリジオイデス・ディフィ
シル抗原陽性かつクロストリジオイデス・ディフィシルト
キシン陰性であること」とされている。
遺伝子検査のほうが抗原検査よりも検出感度が高く,
これまでの方法では見逃していたC. difficileが検出さ
れ,患者本人への診断貢献ばかりではなく,感染制御
的な側面からも利点がある。
【診療ガイドライン中の検査法比較】
Clostridioides difficile感染症診療ガイドラインが2022年に改定され、
本検査の単独使用を認めることとなった。
166