提案書01(0001頁~0202頁)医療技術評価・再評価提案書 (199 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000190899_00011.html |
| 出典情報 | 中央社会保険医療協議会 診療報酬調査専門組織・医療技術評価分科会(令和5年度第1回 11/20)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
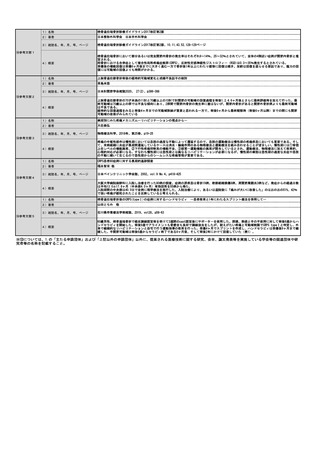
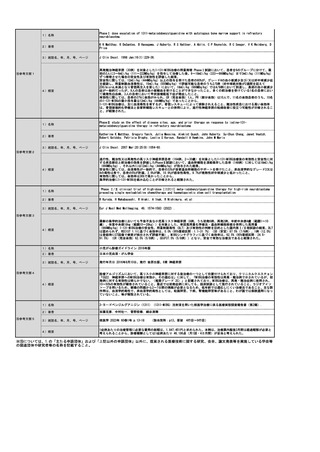
・対象とする患者
・医療技術の内容
・点数や算定の留意事項
・対象とする患者
PET医薬品の効能又は効果に応じた患者となる
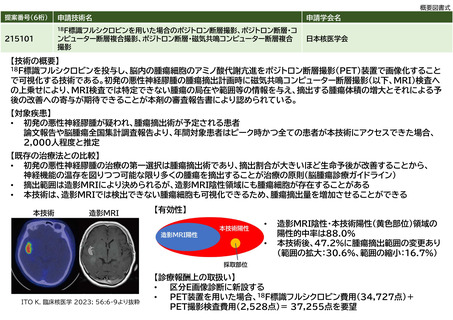
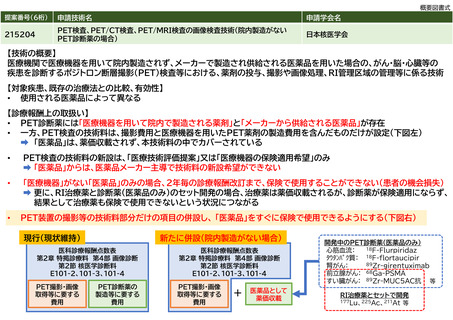
・技術内容
「メーカーから供給される医薬品のみ」のPET医薬品を使用するPET検査である。当該PET医薬品については薬価で取り扱う。技術としては、既存
のPET医薬品を用いた検査と同様となる。具体的には、PET医薬品を投与した後に、PET検査等用の装置を用いて撮影する。撮影後、画像処理を実
施し、画像診断をする。また、PET医薬品の使用にあたっては、放射性物質を取扱う管理区域を管理する。
・点数や算定の留意事項
既存のPET検査等に関わる診療報酬点数には、医療機関内で合成装置(医療機器)を用いてPET薬剤を製造するための費用が含まれていることが前
提となっているが、今回提案する本技術は、既存のPET検査等に関わる診療報酬点数から製造に係る部分を除いた診療報酬点数を追加で設定する
ことである。
E
診療報酬区分(再掲)
診療報酬番号(再掲)
101-2、101-3、101-4
医療技術名
E101-2 ポジトロン断層撮影
4.薬価基準に収載されている医薬品を用いた場合(一連の検査につき)
E101-3 ポジトロン断層・コンピューター断層複合撮影
3.薬価基準に収載されている医薬品を用いた場合(一連の検査につき)
E101-4 ポジトロン断層・磁気共鳴コンピューター断層複合撮影
2.薬価基準に収載されている医薬品を用いた場合(一連の検査につき)
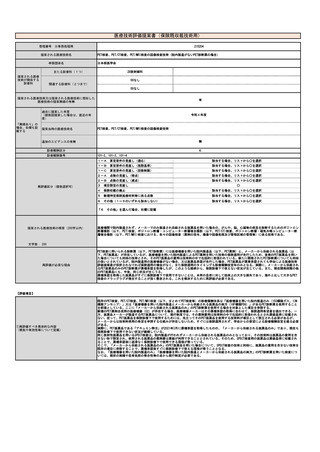
③再評価の根
拠・有効性
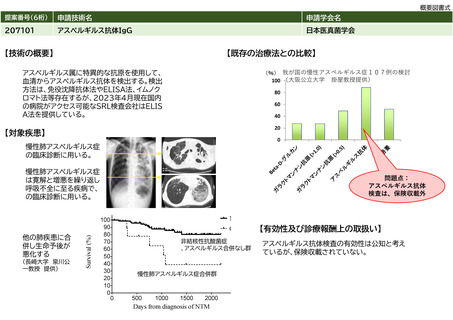
PET検査等自体は、がんや、脳、心臓などの疾患を診断するための有効なツールとして広く使われている(参考文献1)。
治癒率、死亡率やQOLの改善等の長期予 本技術の具体的なアウトカムは、使用されるPET医薬品の効能又は効果による。
PET医薬品は、薬事承認を取得した医薬品となる。すなわち、臨床的有効性や安全性が臨床試験等において確認され、臨床的意義がPMDAに認めら
後等のアウトカム
れたものを用いたPET検査となる
ガイドライン等での位置づけ
④普及性の変化
※下記のように推定した根拠
年間対象者数の
変化
年間実施回数の
変化等
本技術の普及性は、使用するPET医薬品の効能又は効果等による。
見直し前の症例数(人)
使用するPET医薬品による。
見直し後の症例数(人)
使用するPET医薬品による。
見直し前の回数(回)
使用するPET医薬品による。
見直し後の回数(回)
使用するPET医薬品による。
⑤医療技術の成熟度
・学会等における位置づけ
・難易度(専門性等)
・施設基準
(技術の専門性
等を踏まえ、必
要と考えられる
要件を、項目毎
に記載するこ
と)
PET検査等のガイドラインは、必要に応じて、使用するPET医薬品の特性を踏まえて整備さ
ガイドライン等での記載なし(右欄にガイドライン等
れる。
の改訂の見込み等を記載する。)
既存のPET診断薬については、多種のガイドラインにてその有用性が示されている。
PET検査自体は、がん領域等の画像診断として一般的に使用される検査方法である。
位置づけや難易度については、使用するPET医薬品の効能又は効果等による。
以下は、PET検査自体の一般的な要件である。
1. 画像診断を担当する常勤の医師(核医学診断について、相当の経験を有し、かつ、核医学診断に係る研修を受けた者に限る。)が配置されて
施設の要件
(標榜科、手術件数、検査や手術の体 いること。
2. 当該断層撮影を行うにつき十分な機器及び施設を有していること。
制等)
3. 当該断層撮影を行うにつき十分な体制が整備されていること。
以下は、PET検査自体の一般的な要件である。
人的配置の要件
1. 核医学診断の経験を3年以上有し、かつ、日本核医学会が行っているPET核医学検査のための所定の研修を修了した常勤医師が1名以上いるこ
(医師、看護師等の職種や人数、専門 と。
性や経験年数等)
2. 診断撮影機器ごとに、PET製剤の取扱いに関し、専門の知識及び経験を有する専任の診療放射線技師が1名以上いること。
その他
(遵守すべきガイドライン等その他の PET診断薬毎に、必要に応じて適正使用に係るガイドライン等が整備されている。
要件)
⑥安全性
・副作用等のリスクの内容と頻度
PET検査自体は、がん領域等の画像診断として一般的に使用される検査方法であり、安全性に関する懸念はない。
使用されるPET医薬品の安全性については、PMDAに審査され、許容可能と判断されたものとなる。
⑦倫理性・社会的妥当性
(問題点があれば必ず記載)
倫理的な問題はない。
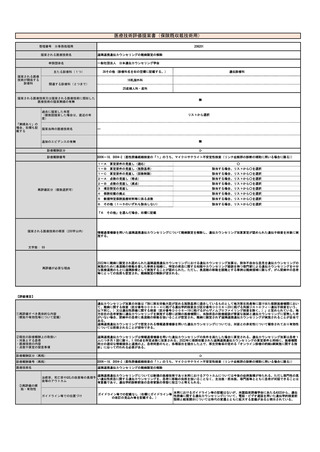
有効性・安全性が臨床試験等により確認され、臨床的意義があると認められ薬事承認を受けた新規の医薬品が、通常であれば原則60日以内、遅く
ても90日以内に薬価基準に収載され保険診療下で使用できるようにも関わらず、PET医薬品のために最低でも2年に1回の診療報酬改定まで使用で
きない状況が継続することは、極めて重大な問題である。本技術により、この問題を解決することは、社会的に妥当である。
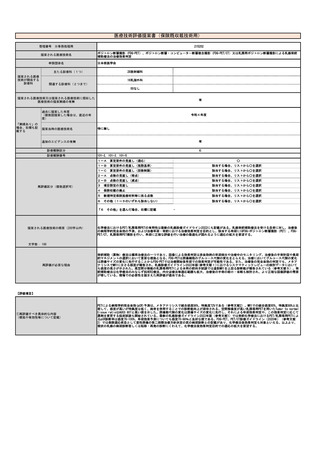
見直し前
E101-2 ポジトロン断層撮影
1. 15O標識ガス剤を用いた場合(一連の検査につき):7,000点
2. 18FDGを用いた場合(一連の検査につき):7,500点
3. 13N標識アンモニア剤を用いた場合(一連の検査につき):9,000点
E101-3 ポジトロン断層・コンピューター断層複合撮影(一連の検査につき)
1. 15O標識ガス剤を用いた場合(一連の検査につき):7,625点
2. 18FDGを用いた場合(一連の検査につき):8,625点
E101-4 ポジトロン断層・磁気共鳴コンピューター断層複合撮影(一連の検査につき):9,160点
見直し後
見直し前の項目に以下を追加する。
E101-2 ポジトロン断層撮影
4. 薬価基準に収載されている医薬品を用いた場合(一連の検査につき):2,528点
E101-3 ポジトロン断層・コンピューター断層複合撮影(一連の検査につき)
3. 薬価基準に収載されている医薬品を用いた場合(一連の検査につき):3,653点
E101-4 ポジトロン断層・磁気共鳴コンピューター断層複合撮影(一連の検査につき)
2. 薬価基準に収載されている医薬品を用いた場合(一連の検査につき):4,188点
その根拠
PET薬剤とPET医薬品の両方が存在するものは、現時点では18FDGのみである。
PET医薬品としての18FDGの販売価格は税込み49,720円(4,972点相当)となっている(放射性医薬品の卸売会社である日本アイソトープ協会の価
格表より)。
既存の点数は、PET薬剤の合成費を含む形で設定されている。PET薬剤費とPET医薬品の購入費が同じとすると、
E101-2 ポジトロン断層撮影の場合
7,500-4,972=2,528点
E101-3 ポジトロン断層・コンピューター断層複合撮影の場合
18FDGを用いた場合(一連の検査につき)
8,625-4,972=3,653点
E101-4 ポジトロン断層・磁気共鳴コンピューター断層複合撮影(一連の検査につき)*
9,160-4,972=4,188点
(*E101-4は18FDGを用いた場合の点数のみが設定されている)
⑧点数等見直し
の場合
199