参考資料 (323 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198111_00025.html |
| 出典情報 | 医療用から要指導・一般用への転用に関する評価検討会議(第27回 3/12)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
7.2 病状が著しい場合及び再発性・難治性の場合に1回20mgを
1日1回投与することができる(再発・再燃を繰り返す逆流性食
道炎の維持療法、プロトンポンプインヒビターによる治療で効
果不十分な場合は除く)。また、プロトンポンプインヒビター
による治療で効果不十分な患者に対し1回10mg又は1回20mgを
1日2回、さらに8週間投与する場合は、内視鏡検査で逆流性食
道炎が治癒していないことを確認すること。なお、本剤1回
20mgの1日2回投与は、内視鏡検査で重度の粘膜傷害を確認し
た場合に限る[17.1.1 参照]。
8. 重要な基本的注意
〈効能共通〉
8.1 本剤の投与中には、血液像や肝機能に注意し、定期的に血液
学的検査・血液生化学的検査を行うことが望ましい。
〈胃潰瘍、十二指腸潰瘍、吻合部潰瘍、非びらん性胃食道逆流症〉
8.2 長期の使用経験が十分でないので、維持療法には用いないこ
とが望ましい。
〈逆流性食道炎の維持療法〉
8.3 再発・再燃を繰り返す患者やプロトンポンプインヒビターに
よる治療で効果不十分な患者に対し行うこととし、本来、維持
療法の必要のない患者に行うことのないよう留意すること。ま
た、食事制限、アルコール摂取制限等の生活習慣の改善が図ら
れ、寛解状態が長期にわたり継続する場合には休薬又は減量を
考慮すること。なお、維持療法中は定期的に内視鏡検査を実施
するなど観察を十分に行うことが望ましい。
〈非びらん性胃食道逆流症〉
8.4 問診により胸やけ、呑酸等の酸逆流症状が繰り返しみられる
こと(1週間あたり2日以上)を確認のうえ投与すること。なお、
本剤の投与が胃癌、食道癌等の悪性腫瘍及び他の消化器疾患に
よる症状を隠蔽することがあるので、内視鏡検査等によりこれ
らの疾患でないことを確認すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 薬物過敏症の既往歴のある患者
9.3 肝機能障害患者
肝硬変患者で肝性脳症の報告がある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には治療上の有益性が
危険性を上回ると判断される場合にのみ投与すること。動物実
験(ラット経口400mg/kg、ウサギ静注30mg/kg)で胎児毒性
(ラットで化骨遅延、ウサギで体重の低下、化骨遅延)が報告
されている。また、ラットにラベプラゾールナトリウム
(25mg/kg/日)、アモキシシリン水和物(400mg/kg/日以上)
及びクラリスロマイシン(50mg/kg/日以上)を4週間併用投与
した試験で、雌で栄養状態の悪化が認められている。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又
は中止を検討すること。動物実験(ラット)で乳汁中へ移行す
ることが報告されている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
消化器症状等の副作用があらわれた場合は休薬するなど慎重に
投与すること。本剤は主として肝臓で代謝されるが、高齢者で
は肝機能が低下していることが多く、副作用があらわれること
がある。
10. 相互作用
本剤の代謝には肝代謝酵素チトクロームP450 2C19
(CYP2C19)及び3A4(CYP3A4)の関与が認められている。
[16.4 参照]
また、本剤の胃酸分泌抑制作用により、併用薬剤の吸収を促進
又は抑制することがある。
10.1 併用禁忌(併用しないこと)
薬剤名等
臨床症状・措置方法
機序・危険因子
アタザナビル硫酸塩 アタザナビルの作用 本剤の胃酸分泌抑制
が減弱するおそれが 作用により、胃内pH
(レイアタッツ)
が上昇し、アタザナ
ある。
[2.2 参照]
ビルの溶解性が低下
し、アタザナビルの
血中濃度が低下する
おそれがある。
リルピビリン塩酸塩 リルピビリン塩酸塩 本剤の胃酸分泌抑制
の作用を減弱するお 作用により、胃内pH
(エジュラント)
が上昇し、リルピビ
それがある。
[2.2 参照]
リン塩酸塩の吸収が
低下し、リルピビリ
ンの血中濃度が低下
することがある。
10.2 併用注意(併用に注意すること)
薬剤名等
ジゴキシン
メチルジゴキシン
臨床症状・措置方法
機序・危険因子
相手薬剤の血中濃度 本剤の胃酸分泌抑制
が上昇することがあ 作用により、胃内pH
が上昇し、相手薬剤
る。
の吸収を促進する。
イトラコナゾール
相手薬剤の血中濃度 本剤の胃酸分泌抑制
ゲフィチニブ
が低下するおそれが 作用により、胃内pH
が上昇し、相手薬剤
ある。
の吸収を抑制するお
それがある。
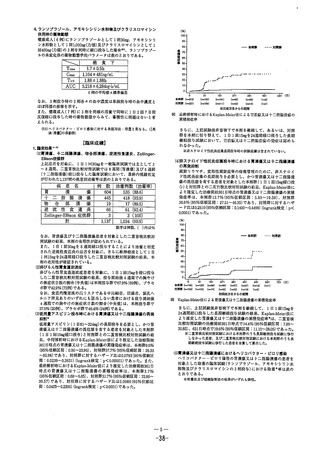
水酸化アルミニウム 本剤単独投与に比べ 機序は不明である。
ゲル・水酸化マグネ 制酸剤同時服用、制
シウム含有の制酸剤 酸 剤 投 与 1 時 間 後 服
用で平均血漿中濃度
曲線下面積がそれぞ
れ8%、6%低下した
との報告がある。
メトトレキサート
メトトレキサートの 機序は不明である。
血中濃度が上昇する
ことがある。高用量
のメトトレキサート
を投与する場合は、
一時的に本剤の投与
を中止することを考
慮すること。
11. 副作用
次の副作用があらわれることがあるので、観察を十分に行い、
異常が認められた場合には投与を中止するなど適切な処置を行
うこと。
11.1 重大な副作用
11.1.1 ショック(頻度不明)、アナフィラキシー(頻度不明)
11.1.2 汎血球減少(頻度不明)、無顆粒球症(頻度不明)、血小
板減少(0.1%未満)、溶血性貧血(頻度不明)
11.1.3 劇症肝炎(頻度不明)、肝機能障害(0.1〜5%未満)、黄疸
(頻度不明)
11.1.4 間質性肺炎(0.1%未満)
発熱、咳嗽、呼吸困難、肺音の異常(捻髪音)等が認められた
場合には、速やかに胸部X線等の検査を実施し、本剤の投与を
中止するとともに、副腎皮質ホルモン剤の投与等の適切な処置
を行うこと。
11.1.5 皮膚障害(頻度不明)
中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、
皮膚粘膜眼症候群(Stevens-Johnson症候群)、多形紅斑等があ
らわれることがある。
11.1.6 急性腎障害(頻度不明)、間質性腎炎(頻度不明)
腎機能検査(BUN、クレアチニン等)に注意すること。
11.1.7 低ナトリウム血症(頻度不明)
11.1.8 横紋筋融解症(頻度不明)
筋肉痛、脱力感、CK上昇、血中及び尿中ミオグロビン上昇を
特徴とする横紋筋融解症があらわれることがある。
11.1.9 視力障害(頻度不明)
11.1.10 錯乱状態(頻度不明)
せん妄、異常行動、失見当識、幻覚、不安、焦燥、攻撃性等が
あらわれることがある。
−2−