参考資料 (325 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198111_00025.html |
| 出典情報 | 医療用から要指導・一般用への転用に関する評価検討会議(第27回 3/12)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
PM(poor metabolizer):CYP2C19*2/*2、CYP2C19*2/*3又
はCYP2C19*3/*3
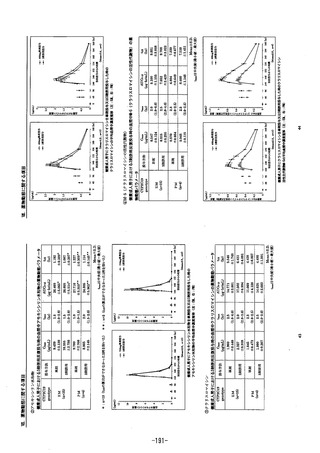
16.1.2 3剤併用投与
健康成人男子にラベプラゾールナトリウム20mg注)、アモキシシ
リン水和物750mg(力価)
、及びクラリスロマイシン400mg(力
価)を1日2回7日間(計12回)反復経口投与した時のラベプラ
ゾールナトリウムの薬物動態パラメータは以下のとおりである。
Zollinger-Ellison症候群については、2例における全般改善度の
改善率は100%であった6)〜14)。
また、H 2受容体拮抗剤抵抗性の逆流性食道炎を対象に1日1回
10mgを24週間投与した維持療法(二重盲検比較試験)におけ
る内視鏡的非再発率は78.6%(33例/42例)であった。
通常用法及び用量のプロトンポンプインヒビター治療に抵抗
性 注1)の逆流性食道炎患者を対象とした投与8週後の内視鏡検
査による治癒率は下表のとおりであった15)。[7.2 参照]
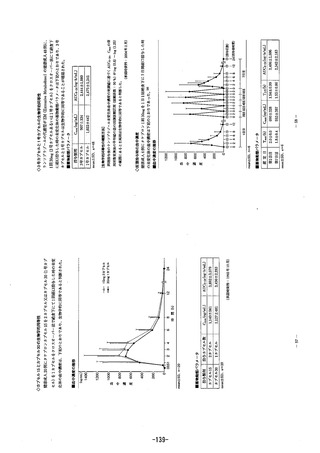
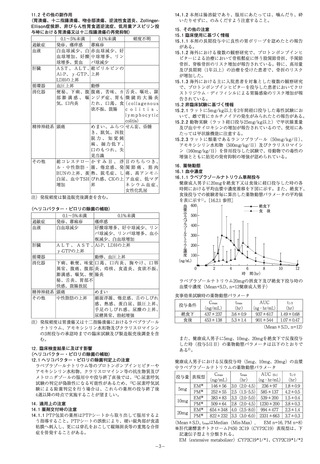
健康成人男子における3剤併用反復投与時の血漿中ラベプラゾー
ルナトリウムの薬物動態パラメータ
1回20mg
1回10mg
1回20mg
1日1回
1日2回
1日2回
58.8%
78.4%
77.0%
全体
(60例/102例) (80例/102例) (77例/100例)
grade A及び
65.1%
87.1%
79.5%
grade B※
(56例/86例) (74例/85例) (66例/83例)
grade C及び
25.0%
35.3%
64.7%
grade D※
(4例/16例) (6例/17例) (11例/17例)
EM※
(n=15)
PM※
(n=4)
Cmax
(ng/mL)
tmax
(hr)
AUC0-12
(ng・hr/mL)
t1/2
(hr)
578±293
3.0±0.7
934±438
0.72±0.19
948±138
2.8±0.5
2600±474
1.80±0.32
(Mean±S.D.)
※肝代謝酵素チトクロームP450 2C19(CYP2C19)表現型は、下
記遺伝子型より分類される。
EM(extensive metabolizer):CYP2C19*1/*1、CYP2C19*1/*2
又はCYP2C19*1/*3
PM(poor metabolizer):CYP2C19*2/*2、CYP2C19*2/*3又
はCYP2C19*3/*3
注)承認用法及び用量は「通常、成人にはラベプラゾールナトリ
ウムとして1回10mg、アモキシシリン水和物として1回
750mg(力価)及びクラリスロマイシンとして1回200mg
(力価)の3剤を同時に1日2回、7日間経口投与する。なお、
クラリスロマイシンは、必要に応じて適宜増量することがで
きる。ただし、1回400mg(力価)1日2回を上限とする。」で
ある。
16.2 吸収
16.2.1 食事の影響
健康成人男子に20mgを絶食下又は食後に経口投与した時、食
後投与では絶食下投与に比しtmaxが1.7時間遅延するとともに吸
収に個体差が認められている1)。[16.1.1 参照]
16.4 代謝
健康成人男子に10mg、20mgを経口投与した時の血漿中の代謝
物は、主に非酵素的な還元反応により生成したチオエーテル体
であった。その他に肝代謝酵素チトクロームP450 2C19
(CYP2C19)が関与する脱メチル化反応により生成した脱メチ
ル体、3A4(CYP3A4)が関与するスルホン化反応により生成
したスルホン体が認められた1),3),4)。[10. 参照]
16.5 排泄
健康成人男子に20mgを経口投与した場合、投与後24時間までに
尿中にラベプラゾールナトリウムの未変化体は検出されず、代
謝物であるカルボン酸体及びそのグルクロン酸抱合体が投与量
の約29〜40%、メルカプツール酸抱合体が13〜19%排泄された3)。
16.7 薬物相互作用
類薬(オメプラゾール)で肝代謝酵素チトクロームP450 2C19
(CYP2C19)への代謝競合により相互作用が認められているジ
アゼパム、ワルファリン(R-ワルファリン)に対して本剤はこ
れらの薬剤の血中濃度に影響を与えないことが報告されている。
また、類薬(ランソプラゾール)で肝代謝酵素チトクローム
P450 1A2(CYP1A2)の誘導により相互作用が認められてい
るテオフィリンに対しても本剤は血中濃度に影響を与えないこ
とが報告されている4),5)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
〈胃潰瘍、十二指腸潰瘍、吻合部潰瘍、逆流性食道炎、ZollingerEllison症候群〉
17.1.1 一般臨床試験及び二重盲検比較試験
胃潰瘍、十二指腸潰瘍、逆流性食道炎及び吻合部潰瘍を対象に
1日1回10mg又は20mgを投与した一般臨床試験及び二重盲検比
較試験(投与期間:6〜8週間)の成績は下表のとおりである。
対象疾患
胃潰瘍
十二指腸潰瘍
逆流性食道炎
吻合部潰瘍
注1)ラベプラゾールナトリウム10mg/日、ランソプラゾール
30mg/日、オメプラゾール20mg/日を8週間以上投与後に未
治癒又は維持療法中に再発
※ロサンゼルス分類(改変2)による重症度
通常用法及び用量のプロトンポンプインヒビター治療に抵抗
性注2)の逆流性食道炎を対象とした維持療法52週投与の内視鏡
検査による非再発率(中央判定)は下表のとおりであった16)。
非再発率の群間差a)
(95%信頼区間)
値b)
投与52週後の
44.8%
73.9%
29.1(18.9, 39.3)
非再発率
(73/163例) (119/161例)
<0.001
1回10mg
1日1回
a)10mg1日2回-10mg1日1回、b)χ2検定
注2)ラベプラゾールナトリウム10mg/日・20mg/日、ランソプ
ラゾール30mg/日、オメプラゾール20mg/日、エソメプラ
ゾール20mg/日を8週間以上投与後に未治癒又は維持療法中
に再発
〈非びらん性胃食道逆流症〉
17.1.2 二重盲検比較試験
非びらん性胃食道逆流症を対象に1日1回10mgを投与した二重
盲検比較試験(投与期間:4週間)における胸やけ症状の完全消
失率及び緩解率は、それぞれ43.6%(44例/101例)、55.4%
(56例/101例)であった。
副作用は、10mg投与の102例中12例(11.8%)に認められた。
主な副作用は、便秘3例(2.9%)及び腹部膨満2例(2.0%)で
あった17)。
〈低用量アスピリン投与時における胃潰瘍又は十二指腸潰瘍の再
発抑制〉
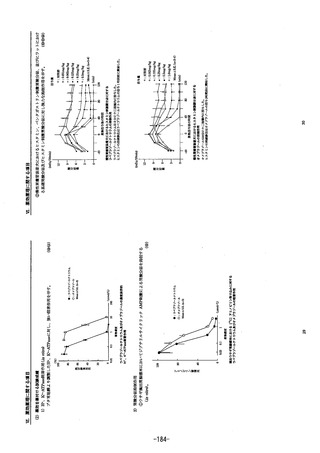
17.1.3 二重盲検比較試験
低用量アスピリン(1日81mg又は100mg)の長期投与を必要と
し、かつ胃潰瘍又は十二指腸潰瘍の既往歴を有する患者を対象
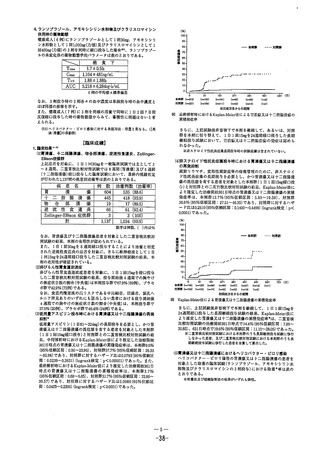
とした二重盲検比較試験の結果、Kaplan-Meier法により推定し
た投与24週間後の胃潰瘍又は十二指腸潰瘍の累積再発率は下表
のとおりであった。
副作用は、本剤10mg投与群で157例中14例(8.9%)、5mg投与
群で156例中7例(4.5%)に認められた。主な副作用は10mg投
与群で下痢及び湿疹各2例(1.3%)、5mg投与群で下痢3例
(1.9%)、肝機能異常2例(1.3%)であった18)。
1日1回5mg
(150例)
4例
再発例数
投与24週後の
2.8%
累積再発率a)
(1.04, 7.17)
(95%信頼区間)
対照に対する
0.11
ハザード比
(0.04, 0.31)
(95%信頼区間)
値b)
<0.001
内視鏡治癒率
95.2%(401例/421例)
98.1%(364例/371例)
90.9%(50例/55例)
83.3%(10例/12例)
1回10mg
1日2回
1日1回10mg
(151例)
2例
対照c)
(151例)
32例
1.4%
21.7%
(0.35, 5.51) (15.84, 29.27)
0.05
(0.01, 0.23)
-
<0.001
-
a)Kaplan-Meier法による推定、b)Log-rank検定、c)対照はテ
プレノン(1回50mg1日3回)
−4−