参考資料 (349 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198111_00025.html |
| 出典情報 | 医療用から要指導・一般用への転用に関する評価検討会議(第27回 3/12)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
15.
1 臨床使用に基づく情報
〈効能共通〉
15.
1.
1本剤の長期投与中に良性の胃ポリープを認めたとの報告が
ある。
15.
1.
2本剤の投与が、胃癌による症状を隠蔽することがあるので、
悪性でないことを確認して投与すること。
15.
1.
3海外における複数の観察研究で、プロトンポンプインヒビ
ターによる治療において骨粗鬆症に伴う股関節骨折、手関節骨折、
脊椎骨折のリスク増加が報告されている。特に、高用量及び長期
間
(1年以上)の治療を受けた患者で、
骨折のリスクが増加した。
15.
1.
4海外における主に入院患者を対象とした複数の観察研究で、
プロトンポンプインヒビターを投与した患者においてクロストリ
ジウム・ディフィシルによる胃腸感染のリスク増加が報告されて
いる。
〈非びらん性胃食道逆流症〉
15.
1.
5食道内酸逆流の高リスクであると考えられる中高齢者、裂孔
ヘルニアを合併する患者のいずれにも該当しない場合には本剤の
治療効果が得られにくい可能性がある。
15.
2 非臨床試験に基づく情報
7mg/kg
15.
2.
1ラットに本剤のラセミ体であるオメプラゾール1.
以上を2年間経口投与した毒性試験で、
胃にカルチノイドの発生が
みられたとの報告がある。このカルチノイドの発生にはラットに
種特異性が認められている。
15.
2.
2ラットに類薬であるランソプラゾール(50mg/kg/日)、アモ
キシシリン水和物(500mg/kg/日)及びクラリスロマイシン
(160mg/kg/日)を併用投与した試験で、母動物での毒性の増強と
ともに胎児の発育抑制の増強が認められている。
16.薬物動態
16.
1 血中濃度
16.
1.
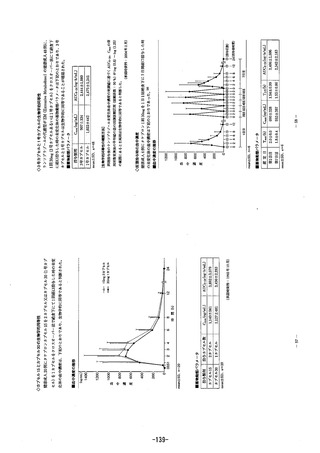
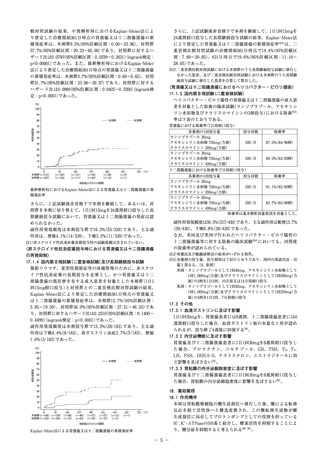
1単回投与
健康成人男性被験者(n=24、CYP2C19のhomo EM、het
er
o EM及び
PM注)が同数)にエソメプラゾール10mg及び20mgを空腹時に単回経口投
与したときの未変化体の薬物動態パラメータは以下のとおりである1)。
Cma(n
/
mL)
x g
Tma(h
)
x r
AUC
(ng・hr
/
mL)
T1/(h
)
2 r
245.
2
10mg
(186.
5328.
1)
2.
50
(1.
005.
00)
552.
6a)
(369.
6822.
1)
1.
05a)
(0.
851.
31)
490.
5
(369.
6645.
9)
2.
75
(0.
756.
00)
1115.
6
(801.
31557.
8)
1.
08
(0.
911.
26)
投与量
20mg
a)n=23
16.
1.
2反復投与
健康成人男性被験者(n=24、CYP2C19のhomo EM、het
er
o EM及び
PM注)が同数)にエソメプラゾール10mg及び20mgを1日1回5日間反復経
口投与したときの第5日目(空腹時投与)の未変化体の薬物動態パラメータ
は以下のとおりである1)。
Cma(n
/
mL)
x g
Tma(h
)
x r
AUC
(ng・hr
/
mL)
T1/(h
)
2 r
10mg
376.
5
(283.
2497.
4)
1.
75
(1.
005.
00)
822.
1a)
(556.
11219.
3)
1.
16a)
(0.
941.
43)
20mg
884.
2
(670.
11167.
5)
2.
25
(1.
004.
00)
2068.
9
(1485.
22880.
6)
1.
25
(1.
061.
46)
12〜14歳
20kg以上
エソメプラゾールの薬物動態パラメータ
1歳以上
10kg以上
20kg未満
10mg
9
1〜11歳
20kg以上
Cmax
a)
(ng/
mL)
AUCτ
a)
(ng・hr
/
mL)
T1/2
c)
(hr
)
854
1.
58
(141.
7%) (1.
035.
92)
2261
(42.
6%)d)
0.
80
±0.
18d)
10mg 10
537
1.
52
(110.
4%) (0.
926.
00)
995
(78.
3%)e)
0.
97
±0.
55e)
20mg 10
1908
(41.
5%)
3459
(50.
9%)
1.
08
±0.
44
b)
)
Tma(h
x r
1.
47
(0.
931.
52)
b)
Tma(h
)
x r
AUCτ
a)
(ng・hr
/
mL)
T1/2
c)
(hr
)
9
311
(91.
7%)
1.
57
(0.
932.
95)
619
(105.
5%)
1.
37
±0.
88
20mg 10
981
(51.
3%)
1.
75
(0.
953.
00)
1918
(33.
6%)
1.
06
±0.
25
16.
3 分布
16.
3.
1血漿蛋白結合
n
エソメプラゾール(添加濃度:2又は20µmol
/L)のヒト血漿蛋白結合率(i
vi
t
r
o)は97%であった4)。
16.
4 代謝
i
n vi
t
r
o肝代謝試験の結果から、ヒドロキシ体、5O脱メチル体の生成に
はCYP2C19、スルホン体の生成にはCYP3A4が関与し、これら3種の代謝
物への代謝クリアランスは同程度であると報告されている 3)。エソメプラ
ゾールのi
n vi
t
r
o肝代謝において、ヒドロキシ体及び5O脱メチル体の生
成に関与するCYP2C19の寄与率(代謝固有クリアランス:CLint)は73%で
あった3)。外国人のデータでは、健康成人に14C標識エソメプラゾールを単回
経口投与したとき、血漿中の主代謝物はスルホン体及びヒドロキシ体で
あった4)。
[9.
3、
10.
参照]
16.
5 排泄
外国人のデータでは、14C標識エソメプラゾールを単回経口投与したとき、
投与放射能の約95%が48時間までに尿中及び糞中に排泄され、尿中排泄量
と糞便中排泄量の比は約4対1であった4)。
16.
6 特定の背景を有する患者
16.
6.
1高齢者
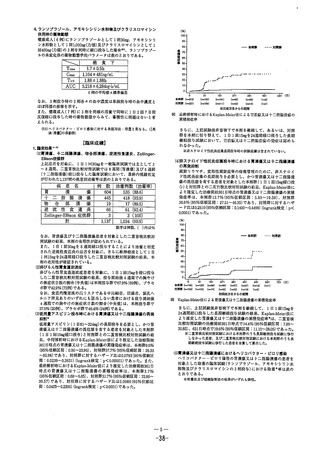
外国人のデータでは、エソメプラゾールを健康高齢被験者に1日1回5日間反
復経口投与したとき、投与5日目のAUC及びCmaxは非高齢の症候性胃食道
逆流症患者よりも高い傾向を示し、幾何平均の比(健康高齢/非高齢患者)
は各々1.
25
(95%信頼区間:0.
941.
67)
、
1.
18
(同:0.
911.
52)
であった5)。
16.
6.
2肝機能障害患者
外国人のデータでは、エソメプラゾールを肝機能障害患者に1日1回5日間反
復経口投与したとき、AUCτは、肝機能低下のない症候性胃食道逆流症患者
に比べ、重度の肝機能障害患者では約2.
3倍高く、軽度〜中程度の肝機能障
害患者でもその比は1.
4〜1.
8であった6)。
16.
7.
1ジアゼパム、
フェニトイン又はワルファリン
発現系CYP2C19及びヒト肝ミクロソームを用いるi
n vi
t
r
o試験において
本薬はCYP2C19の活性を阻害した(Ki
値:7.
9及び8.
6µM)が、CYP2A6、
CYP1A2、CYP2D6、CYP2E1、CYP2C9及びCYP3A4の活性については阻
8)
害しないかわずかな阻害作用を示した7),
。
外国人のデータでは、ジアゼパム、フェニトイン又はワルファリン(R ワル
ファリン)
(以上、CYP2C19の基質)と本剤の併用により、ジアゼパム、フェ
ニトインのAUCはそれぞれ81%、13%増大し、Rワルファリンの血漿中ト
ラフ濃度は13%上昇した9)。
[10.
2参照]
16.
7.
2その他の薬剤
エソメプラゾールとクラリスロマイシン及びアモキシシリン水和物の併用
により、クラリスロマイシン及びアモキシシリン水和物の血漿中濃度に影
響しなかったが、クラリスロマイシンの14位水酸化代謝物のAUCτは増大
した。また、エソメプラゾールのAUCτは非併用時の約2倍に増大した9)。キ
投与3日目及び5日目のCmaxは同程度であったことから、反復投与開始後3
日には血漿中エソメプラゾール濃度は定常状態に到達したと考えられた。
投与5日目の投与後12時間における血漿中エソメプラゾール濃度はほぼ検
出限界以下に低下し、
1日1回反復投与しても累積は認められなかった1)。
16.
1.
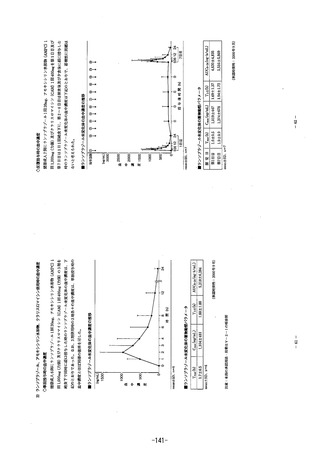
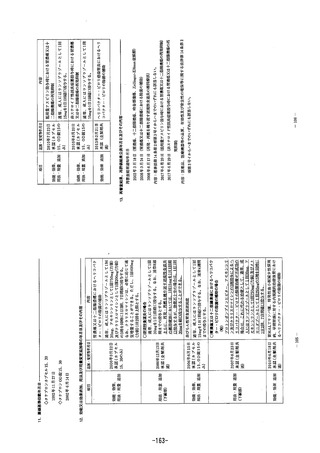
3幼児及び小児
幼児及び小児患者にエソメプラゾール10mg及び20mgを1日1回5日間以上
反復経口投与したところ、未変化体の薬物動態パラメータは以下のとおり
であった2)。
n
10mg
Cmax
a)
(ng/
mL)
注)
homo EM:CYP2C19*
1/
*
1
het
er
o EM:CYP2C19*
1/
*
2又はCYP2C19*
1/
*
3
PM:CYP2C19*
2/
*
2、
CYP2C19*
2/
*
3又はCYP2C19*
3/
*
3
ニジン9)、ナプロキセン10)、ロキソプロフェンナトリウム11)、アスピリン12)
と本剤の併用では相互作用は認められなかった。
a)n=23
投与量
n
a)幾何平均値
(変動係数) b)中央値
(最小値−最大値)
c)平均値±標準偏差 d)n=7 e)n=9
Tmaxは中央値
(最小値−最大値)
、
それ以外は幾何平均(95%信頼区間)
、
被験者の
年齢及び体重
エソメプラゾールの薬物動態パラメータ
投与量
16.
7 薬物相互作用
Tmaxは中央値
(最小値−最大値)
、
それ以外は幾何平均(95%信頼区間)
、
投与量
被験者の
年齢及び体重
17.臨床成績
17.
1 有効性及び安全性に関する試験
〈逆流性食道炎〉
17.
1.
1国内第I
I
I
相試験(成人)
逆流性食道炎を対象とした二重盲検比較試験では、オメプラゾール20mg、
エソメプラゾール20mg又は40mgが1日1回最大8週間投与され、投与8週時
のそれぞれの治癒率[95%信頼区間]は87.
4%
(166/190例)
[ 81.
9%、
91.
4%]、87.
3%
(165/189例)
[ 81.
8%、91.
3%]及び90.
0%
(171/190例)
[84.
9%、93.
5%]であり、オメプラゾール20mgに対する本剤20mg及び
40mgの非劣性が認められている13)。
副作用発現頻度は、エソメプラゾール20mg群で7.
9%
(15/189例)であっ
た。主な副作用は下痢2例(1.
1%)、アラニン・アミノトランスフェラーゼ増
加2例(1.
1%)及び血中クレアチンホスホキナーゼ増加2例(1.
1%)であっ
た。
17.
1.
2国内第I
I
I
相試験(成人)
逆流性食道炎の治癒患者を対象とした二重盲検比較試験において、オメプ
ラゾール10mgと比較したエソメプラゾール10mg及び20mgの1日1回24
週間投与時における逆流性食道炎の再発抑制効果が認められている14)。
−4−