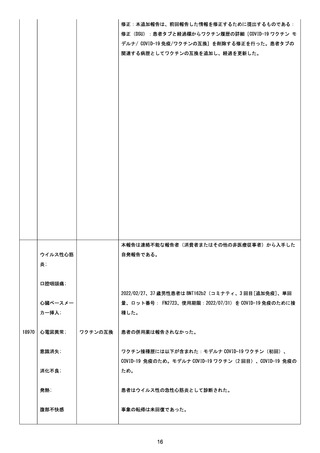
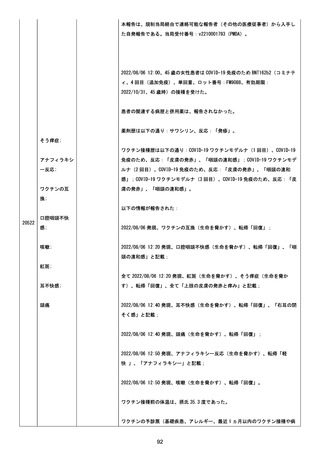
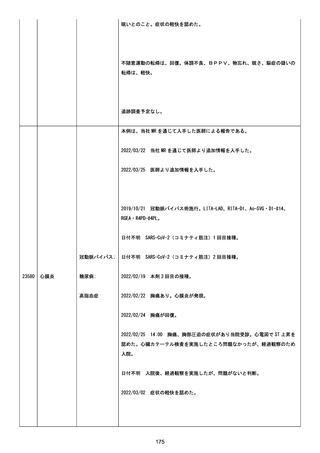
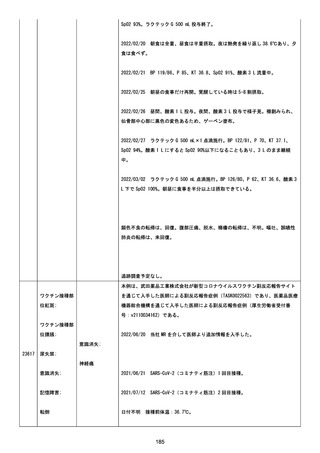
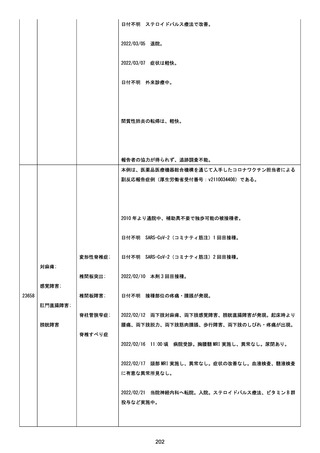
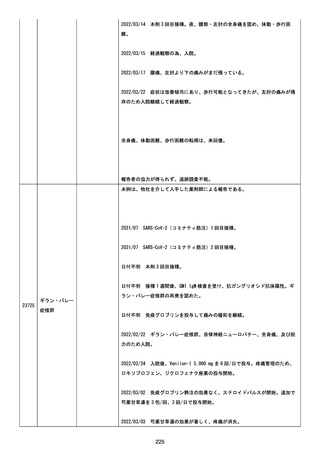
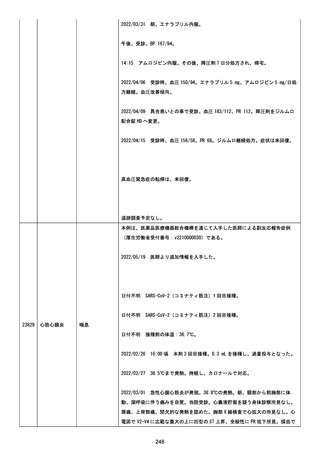
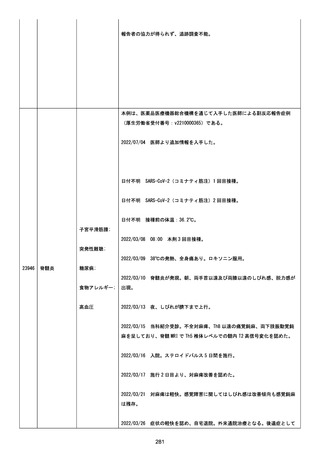
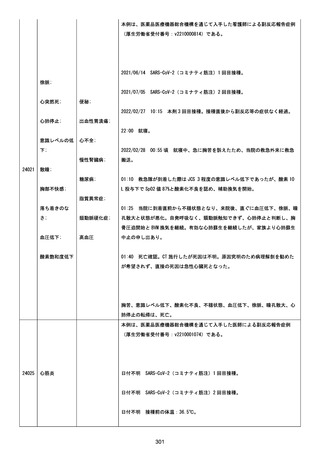
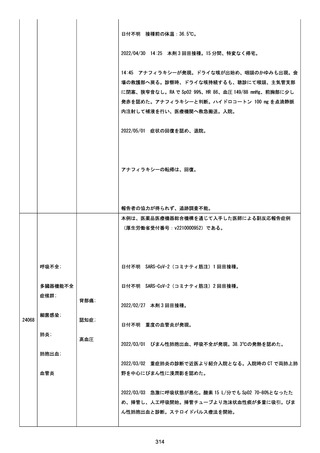
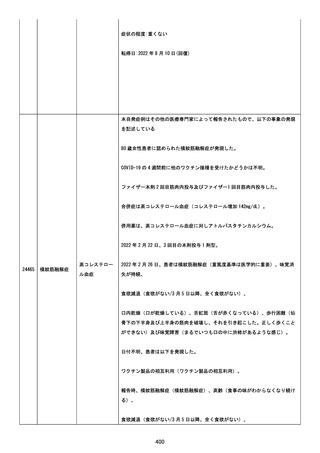
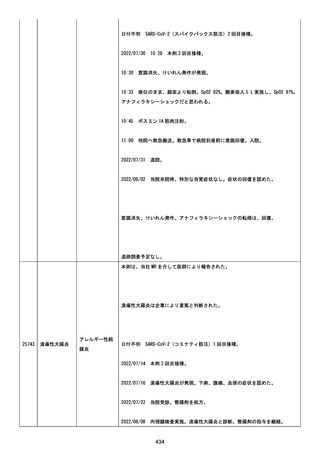
資料1-2-3-6 薬機法に基づく製造販売業者からの副反応疑い報告状況について(交互接種に係る報告症例・基礎疾患等及び症例経過) (71 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00055.html |
| 出典情報 | 第 88 回厚生科学審議会予防接種・ワクチン分科会 副反応検討部会、令和4年度第 18 回薬事・食品衛生審 議会薬事分科会医薬品等安全対策部会安全対策調査会(11/11)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
コロナに感染して抗体が出来ているかもしれないので、4回目接種をする必要が
あるのか。
結論:本ロットに関して、有害事象安全性調査要請および/または効果の欠如につ
いてはすでに調査された。当該バッチの出荷後 6 ヵ月以内に苦情を受けたため、
苦情サンプルは活性成分の量を測定するために測定管理室に送られなかった。す
べての分析結果は確認され、予め定められた範囲内であった。当該 PR ID の調査
の結果、以下の結論となった:参考 PR ID 6099040。
「PFIZER-BIONTECH COVID-19VACCINE」の苦情が調査された。
調査には、関連するバッチ記録の確認、逸脱調査、報告されたロットと製品タイ
プの苦情履歴の分析が含まれた。最終的範囲は、報告されたロット FC8736 の関連
ロットと決定された。苦情サンプルは、返却されなかった。調査中に関連する品
質問題は特定されなかった。製品の品質、規制、検証および安定性への影響はな
かった。プールス製造所は、報告された欠陥はバッチ全体の品質の典型的なもの
ではなく、バッチは引き続き許容できると結論付けた。NTM プロセスは、規制当
局への通知は不要と判断した。報告された欠陥は確認することができなかった。
苦情は確認されなかったため、根本原因または CAPA は特定されなかった。
結論:調査には、関連するパッチ記録の確認、逸脱検査および報告されたロット
と製品タイプの苦情履歴の分析が含まれた。最終的な範囲は、報告されたロット
EY5420 の関連ロットと決定された。苦情サンプルは返却されなかった。
調査中、関連する品質問題は特定されなかった。
製品品質、規制、バリデーションおよび安定性への影響はなかった。
プールス製造所は、報告された欠陥がバッチの品質の典型的なものではなく、バ
ッチは引き続き許容できると結論付けた。
NTM プロセスは、規制当局への通知は不要と判断した。
報告された欠陥は確認することができなかった。苦情が確認されなかったため、
根本原因または CAPA は特定されなかった。
71