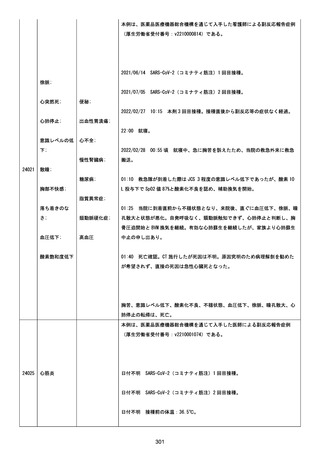
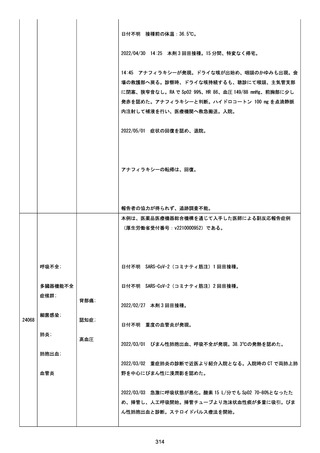
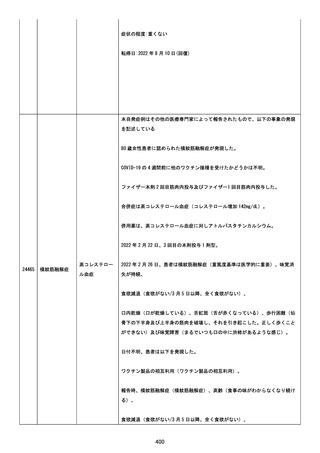
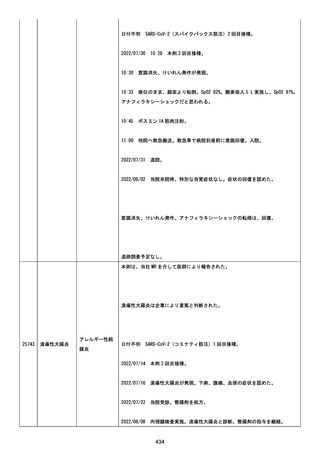
資料1-2-3-6 薬機法に基づく製造販売業者からの副反応疑い報告状況について(交互接種に係る報告症例・基礎疾患等及び症例経過) (93 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00055.html |
| 出典情報 | 第 88 回厚生科学審議会予防接種・ワクチン分科会 副反応検討部会、令和4年度第 18 回薬事・食品衛生審 議会薬事分科会医薬品等安全対策部会安全対策調査会(11/11)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
1~3 回目のモデルナワクチン接種後にいずれも皮膚の発赤と咽頭の違和感を呈し
た。サワシリンで発疹の既往があった。
2022/08/06 12:20、患者は有害事象を発現した。
事象の経過は以下のとおり:
ファイザーワクチンを初めて接種し、20 分後から上肢の皮膚の発赤と痒み、咽頭
の違和感を発現した。12:22、フェキソフェナジン 120mg を内服し、経過観察し
た。
上記の症状は軽快傾向となったが、12:40 頃から頭痛、右耳の閉そく感を発現
し、12:50 から咳嗽が出現し、アナフィラキシーを発現したと判断し、12:52 にア
ドレナリン 0.3 mg を左大腿に筋注した。収縮期血圧は 140 mmHg で、血圧低下は
認められなかった。アドレナリン筋注後 10 分以内に、すべての症状は消失した。
重大な有害事象であったため、救急要請した。
2022/08/06、事象の転帰は軽快であった(報告どおり)。
報告したその他の医療従事者は、事象を重篤(生命を脅かす)とし、事象と
bnt162b2 との因果関係を関連ありと評価した。他の要因(他の疾患など)の可能
性はなかった。
報告したその他の医療従事者の意見は以下のとおり:
ワクチン接種からアナフィラキシーの発症までの時間が予想以上に長かった。し
たがって、経過観察を十分時間を取る必要があると感じた。本報告は、アナフィ
ラキシーの基準を満たしている(50 分)。事象「アナフィラキシー」、「上肢の
皮膚の発赤と痒み」、「咽頭の違和感」、「頭痛」、「右耳の閉そく感」、「咳
嗽」は、緊急治療室受診を必要とした。
患者は以下の検査および処置を受けた:血圧測定:(2022/08/06)、収縮期血圧
は 140 であった、注記:収縮期血圧は 140mmHg で、血圧低下は認められなかっ
た;体温:(2022/08/06)摂氏 35.3 度、注記:ワクチン接種前。
アナフィラキシー反応、紅斑、そう痒症、口腔咽頭不快感、頭痛、耳不快感、咳
嗽の結果として治療的な処置がとられた。
93