ガイドライン (230 ページ)
出典
| 公開元URL | https://www.caicm.go.jp/action/plan/index.html#influenza_initial_response_guideline |
| 出典情報 | 新型インフルエンザ等対策政府行動計画ガイドライン(8/30)《内閣感染症危機管理統括庁》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
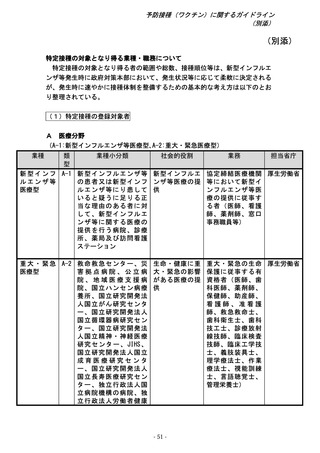
(第3章 初動期における対応)
政府対策本部に報告する。
② 平時に行われた研究における、プレパンデミックワクチン既接種者
の保存血清と発生した新型インフルエンザのウイルス株の交さ免疫性
の調査の結果等に基づき、発生した新型インフルエンザの抗原性等を
評価した上で、厚生労働省はプレパンデミックワクチンの有効性が期
待できるかどうか早期に判断することとする。
なお、発生した新型インフルエンザのウイルスの亜型が異なる、抗
原性が大きく異なるなど、有効性が期待できない場合には、プレパン
デミックワクチンの接種を行わない。
③ 厚生労働省は、プレパンデミックワクチンについて、必要な薬事上
の対応を実施する。
④ 厚生労働省は、最も有効性が期待されるプレパンデミックワクチン
の選択後、あらかじめ製剤化していた当該ワクチンを接種できるよう
関係機関に周知する。
⑤ 厚生労働省は、備蓄していた当該ワクチン原液について、季節性イ
ンフルエンザワクチンなど他のワクチンに優先して迅速に製剤化を行
うよう、ワクチン製造販売業者に依頼する。
⑥ 早期の供給を図るために、供給バイアルサイズは 10ml 等のマルチバ
イアルを主とする(集団的な接種を基本とする。)。なお、各接種会場
における端数の人数及び小規模な医療機関の医療従事者への接種等に
対応するため、一定程度は1ml 等の小さなバイアルを確保する。
⑦ 新型インフルエンザ発生時には、感染拡大の状況等も勘案しつつ、
緊急に使用される必要性があるため検定を受けるいとまがない場合に
は、厚生労働省は、適切に品質を確保することを前提として、必要に
応じプレパンデミックワクチンの検定を免除する。
(2)パンデミックワクチン(第3部第7章 2-2-2)
① 発生時のパンデミックワクチンの確保(国内での製造)
a 厚生労働省は、パンデミックワクチンの生産に当たっては、以下
について取り組む。
ⅰ 通常、集団的な接種が想定されることを念頭に、短期間でより多
くの接種回数分の製品を出荷できるよう、製剤の形態を選択するよ
うワクチン製造販売業者に要請する。
ⅱ 病原性等を踏まえて想定される接種者数・接種回数を考慮して、
厚生労働省は、ワクチン製造販売業者に、必要な製造量を示すとと
もに、状況の変化に応じて、製造量を調整する。
- 26 -