医療機器不具合報告 (37 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000190382_00013.html |
| 出典情報 | 薬事・食品衛生審議会 医療機器・再生医療等製品安全対策部会(令和5年度第1回 7/20)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
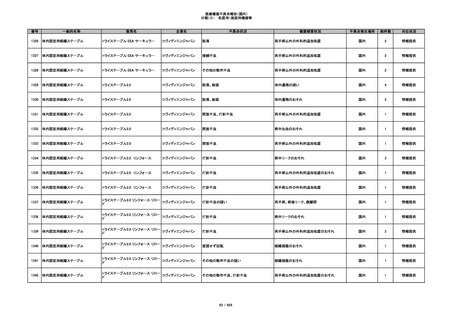
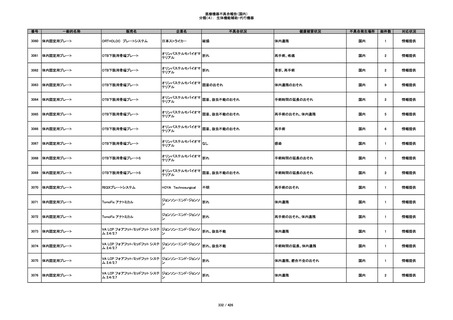
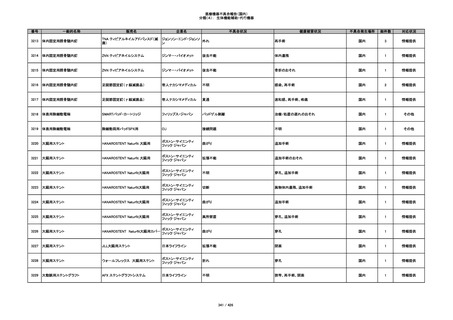
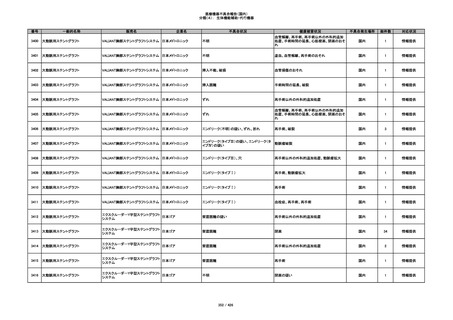
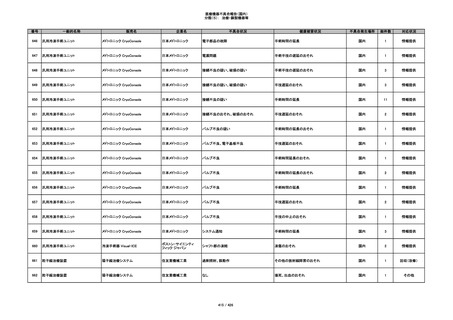
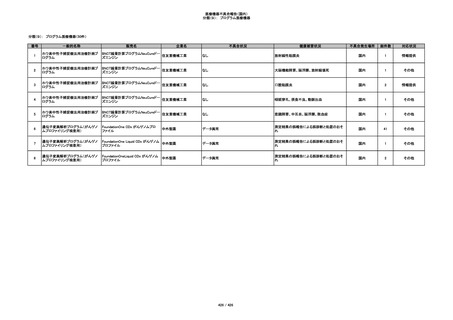
分類(3): 処置用・施設用機器等
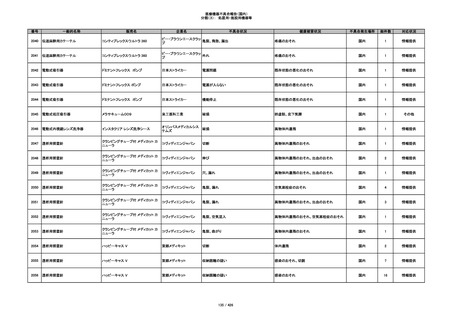
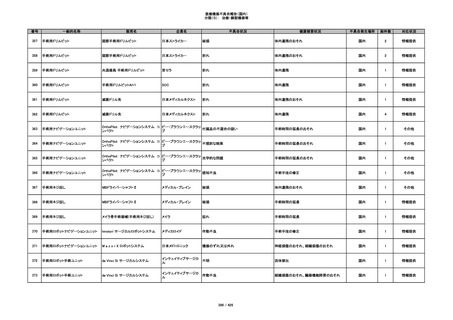
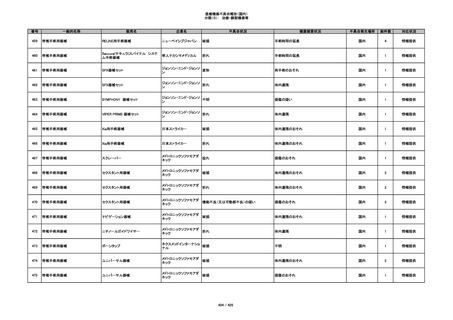
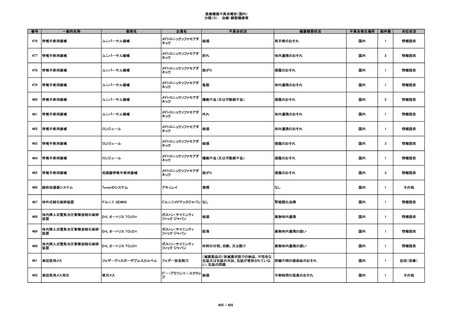
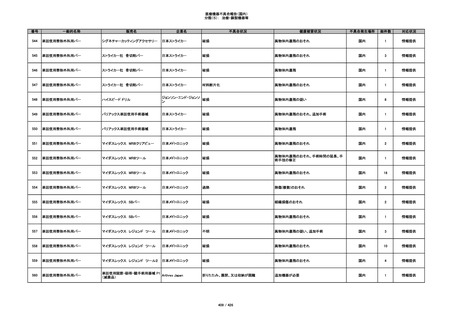
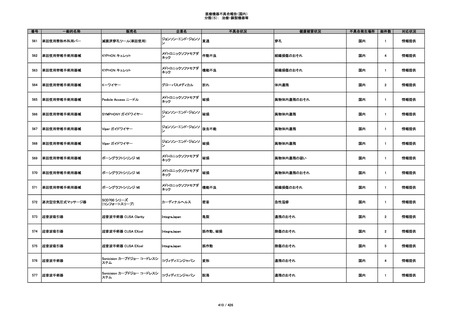
番号
一般的名称
販売名
企業名
不具合状況
健康被害状況
不具合発生場所
総件数
対応状況
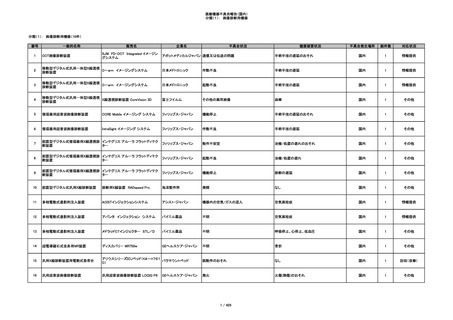
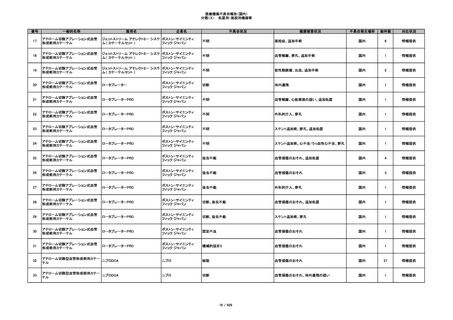
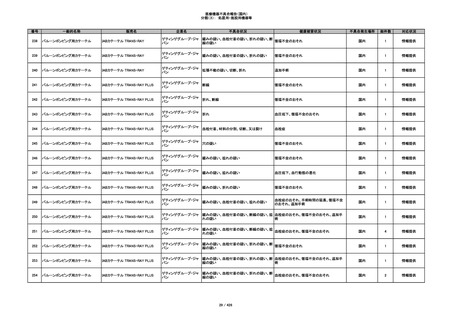
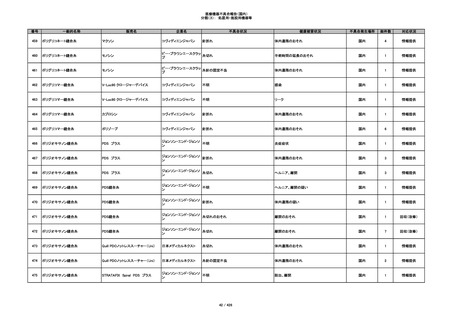
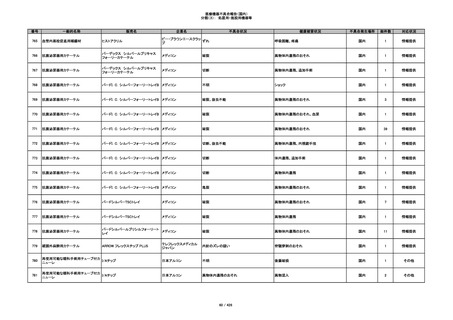
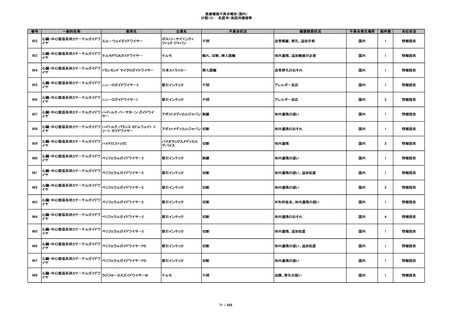
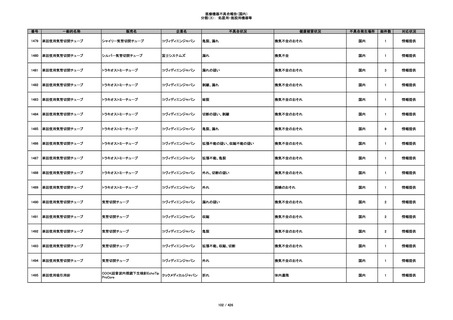
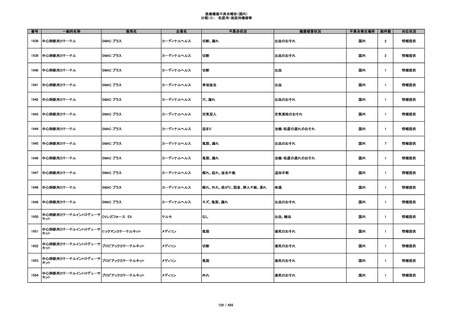
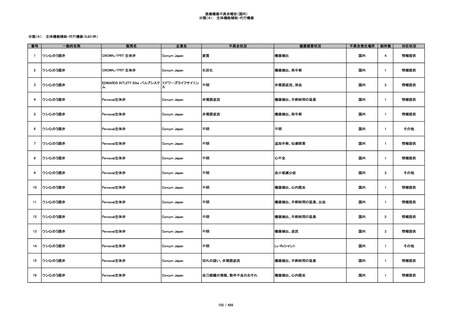
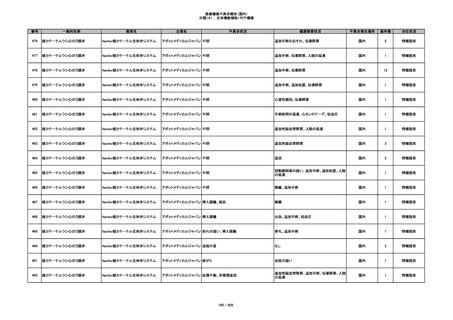
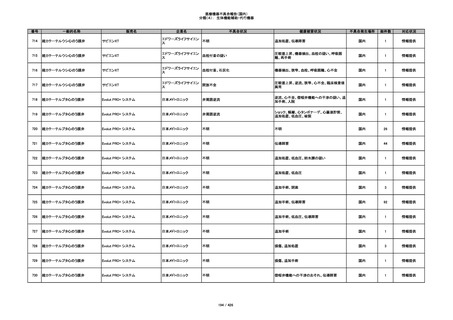
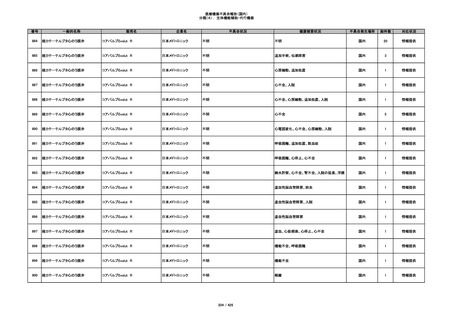
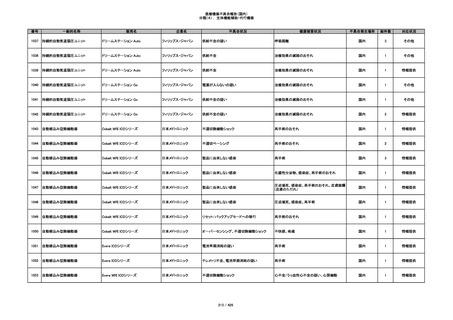
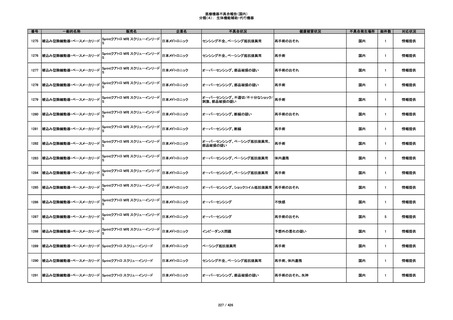
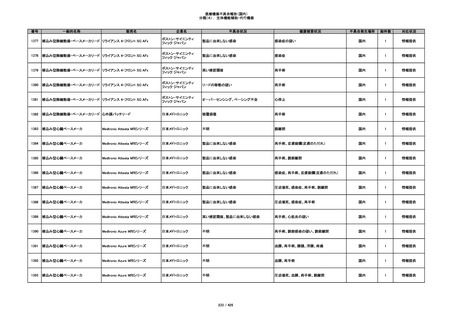
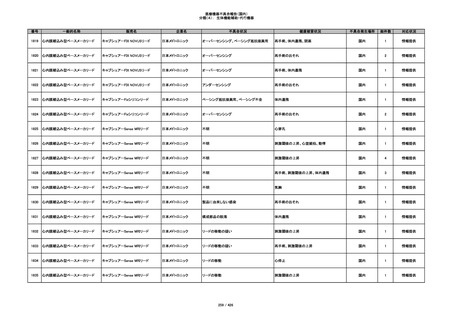
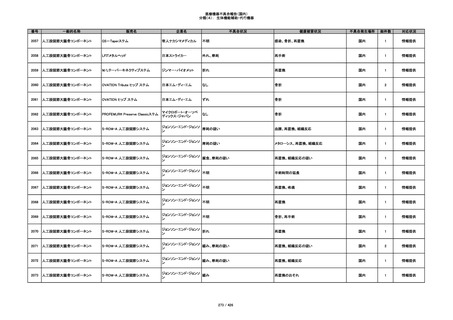
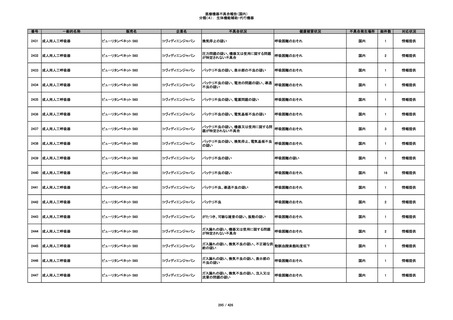
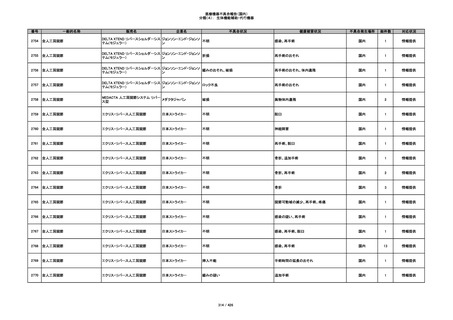
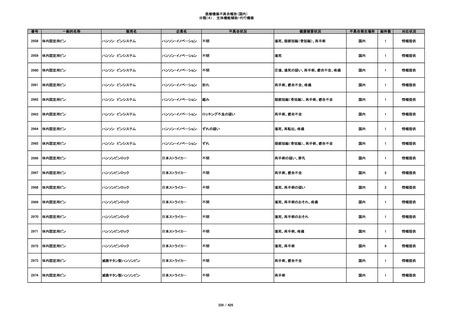
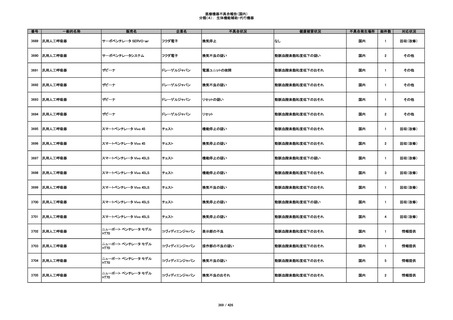
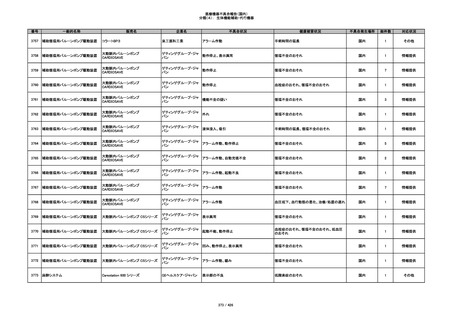
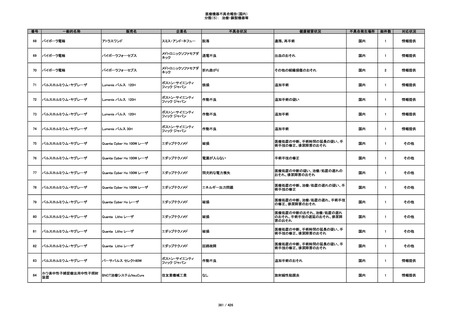
340
ヒアルロン酸使用軟組織注入材
ジュビダームビスタ ボリューマXC
アラガン・ジャパン
不明
血管塞栓
国内
1
情報提供
341
ヒアルロン酸使用軟組織注入材
ジュビダームビスタ ボリューマXC
アラガン・ジャパン
不明
感染
国内
1
情報提供
342
ヒアルロン酸使用軟組織注入材
ジュビダームビスタ ボリューマXC
アラガン・ジャパン
不明
炎症反応
国内
1
情報提供
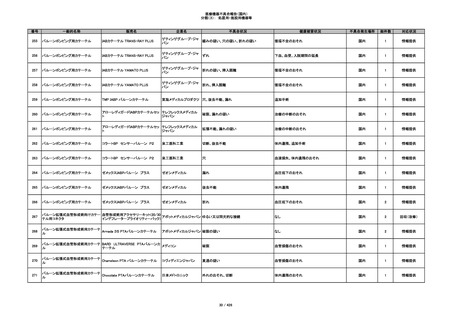
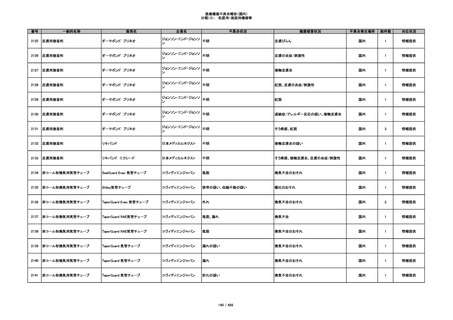
343
ヒアルロン酸使用軟組織注入材
ジュビダームビスタ ボリューマXC
アラガン・ジャパン
不明
インフルエンザ様症状、劇症肝炎の疑い、疼痛
国内
1
その他
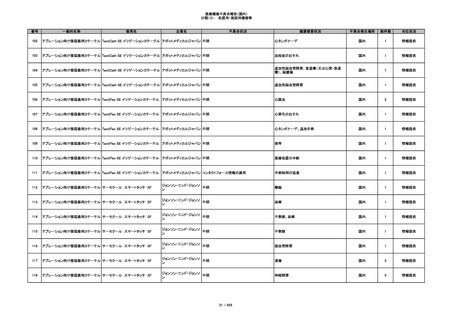
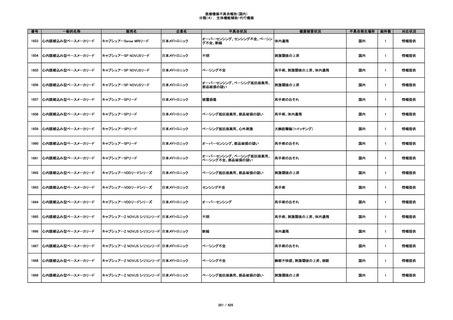
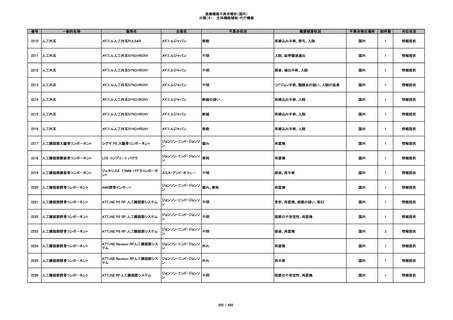
344
ヒアルロン酸使用軟組織注入材
ジュビダームビスタ ボリューマXC
アラガン・ジャパン
不明
アレルギー反応の疑い、インフルエンザ様症
状、感覚異常、呼吸困難、視力障害、出血、頭
痛、変色
国内
1
情報提供
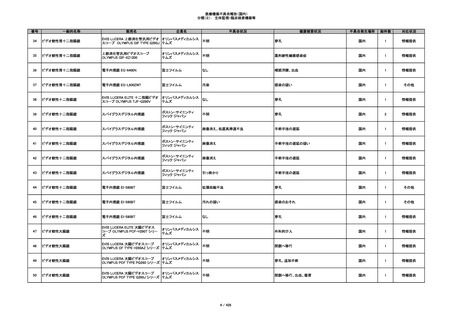
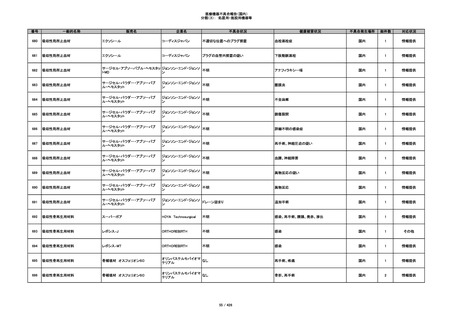
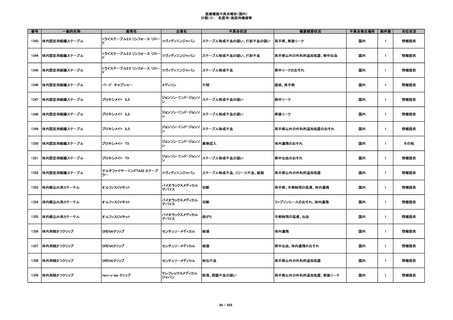
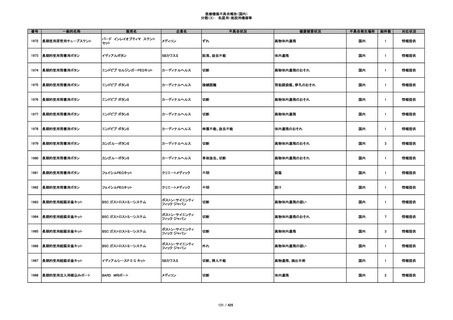
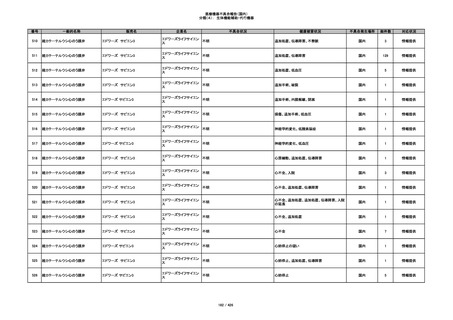
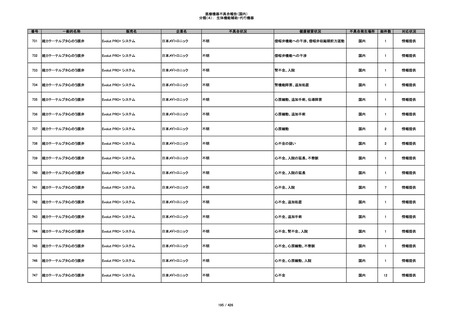
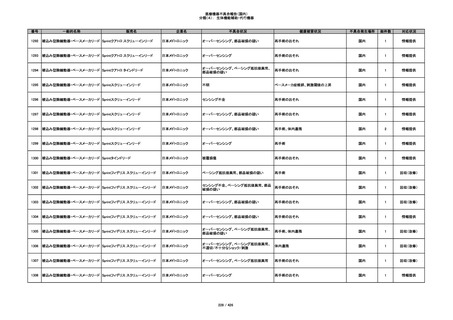
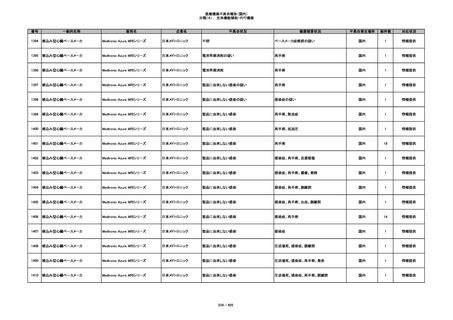
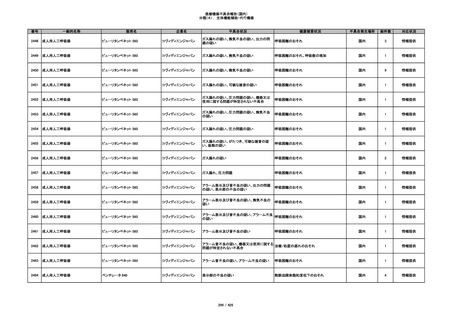
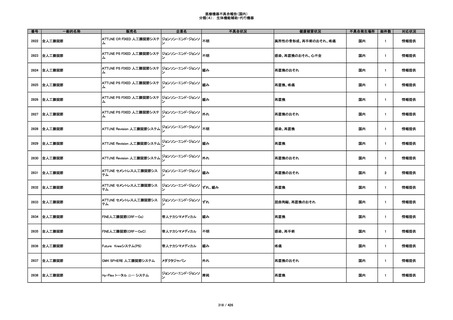
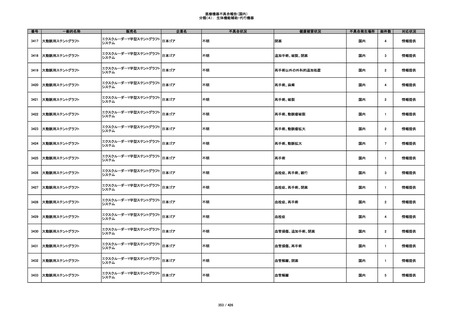
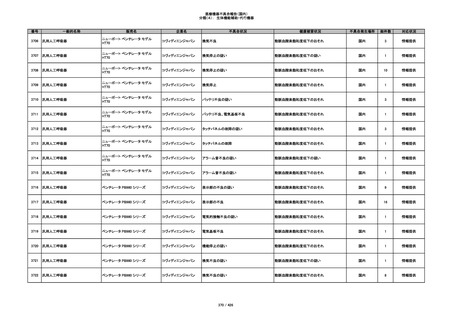
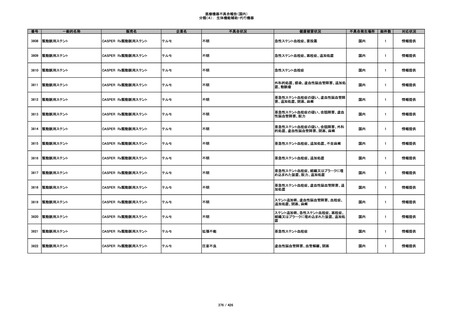
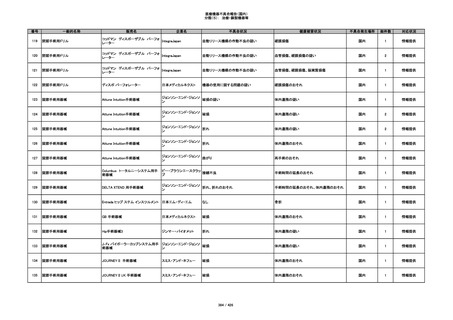
345
ヒアルロン酸使用軟組織注入材
ジュビダームビスタ ボルベラXC
アラガン・ジャパン
不明
塞栓の疑い
国内
1
情報提供
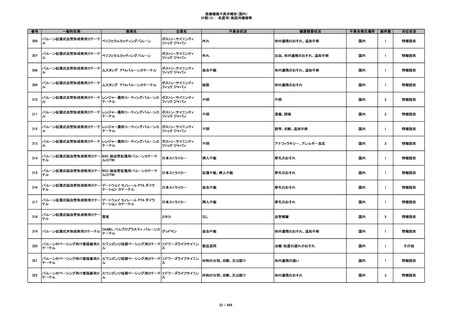
346
ヒアルロン酸使用軟組織注入材
ジュビダームビスタ ボルベラXC
アラガン・ジャパン
不明
血管閉塞
国内
1
情報提供
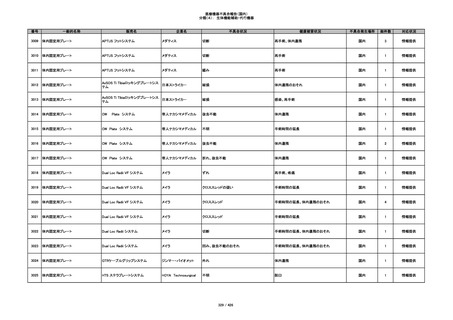
347
ヒアルロン酸使用軟組織注入材
ジュビダームビスタ ボルベラXC
アラガン・ジャパン
不明
急性結膜炎
国内
1
その他
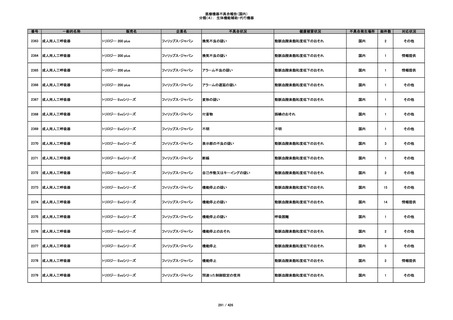
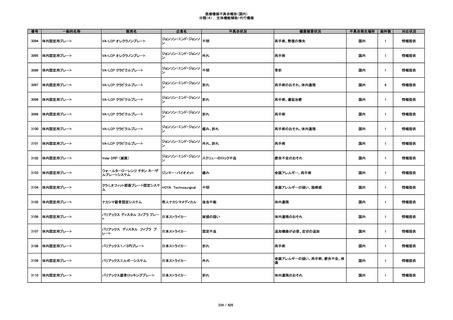
348
ヒアルロン酸使用軟組織注入材
ジュビダームビスタ ボルベラXC
アラガン・ジャパン
不明
感染
国内
4
情報提供
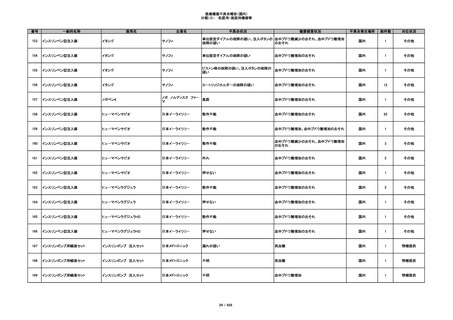
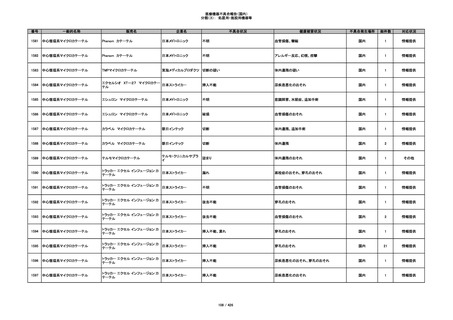
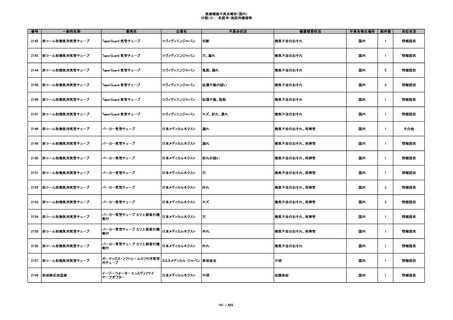
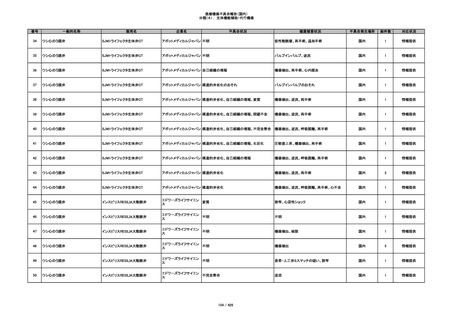
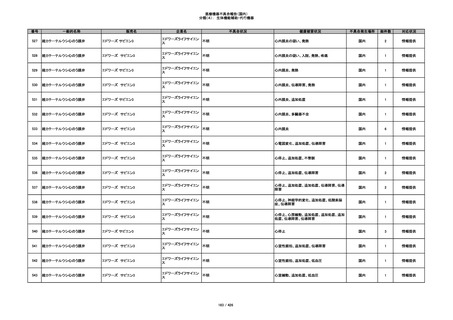
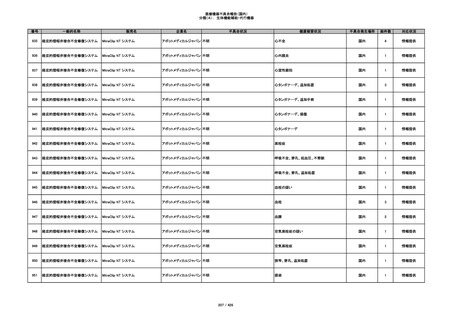
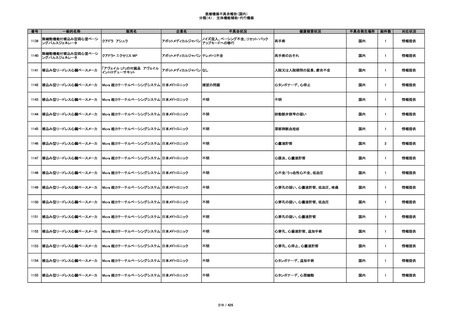
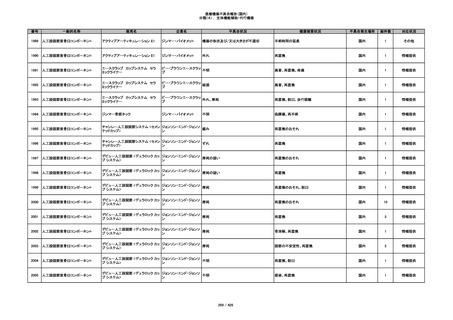
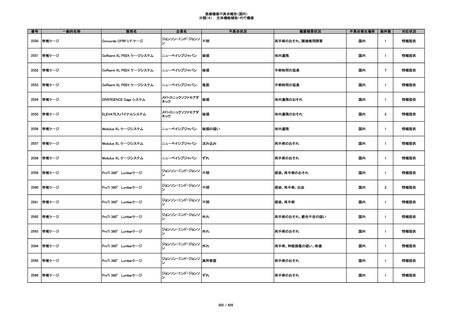
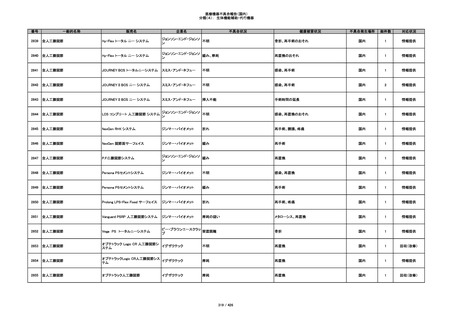
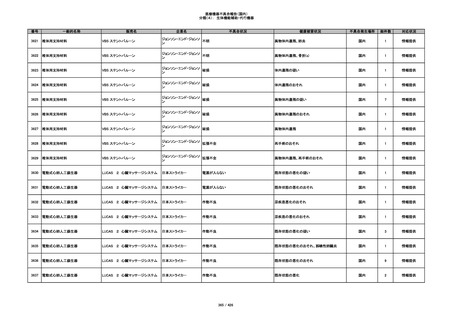
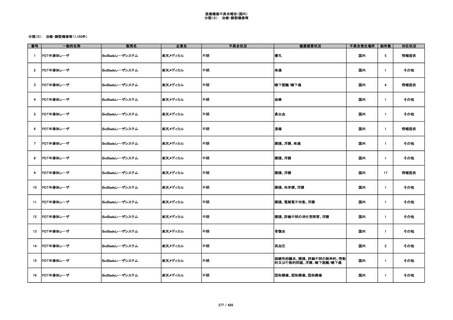
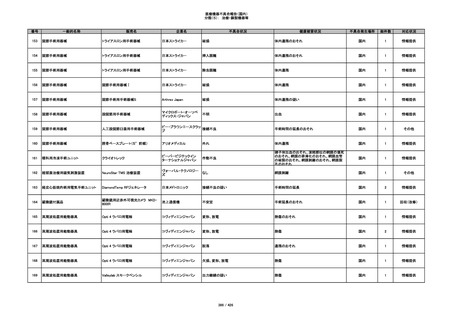
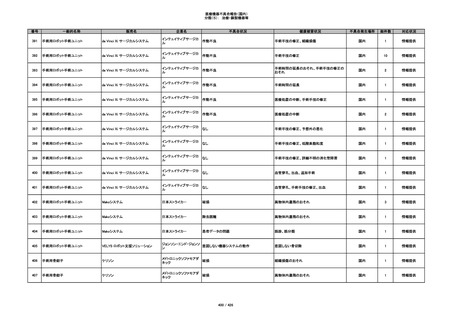
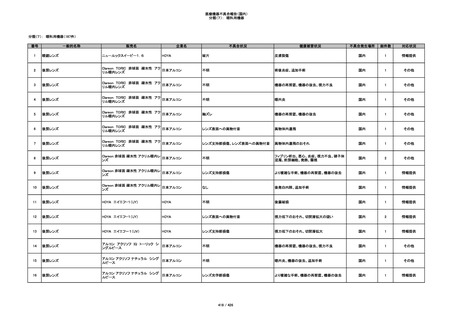
349
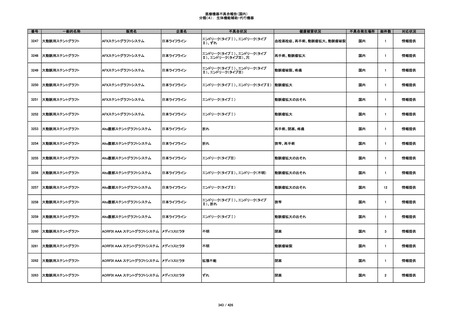
ヒト脱灰骨基質使用吸収性骨再生用材
グラフトンDBM
料
メドトロニックソファモアダ
不明
ネック
感染
国内
1
情報提供
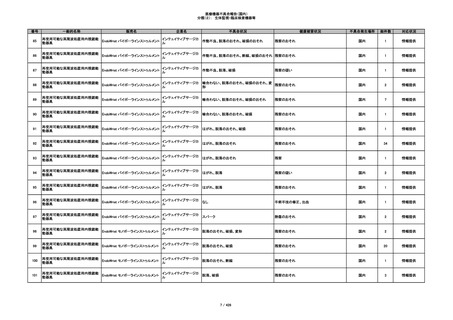
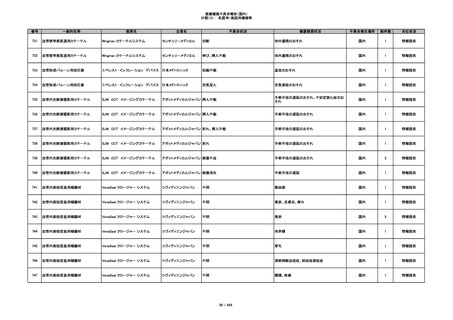
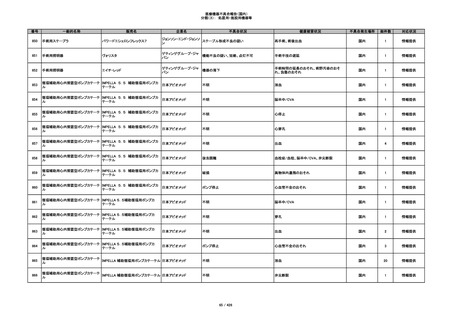
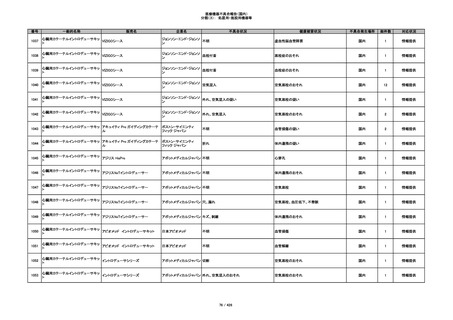
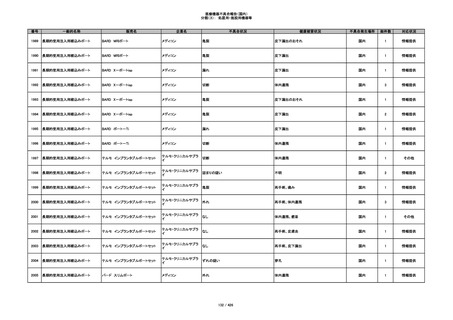
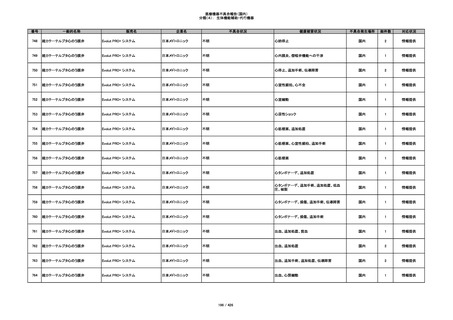
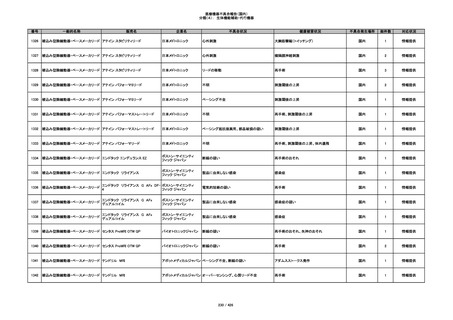
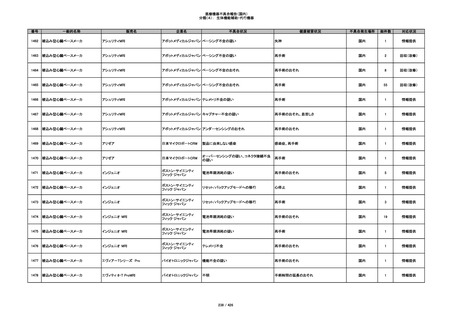
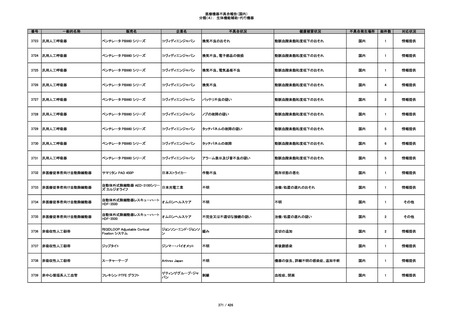
350
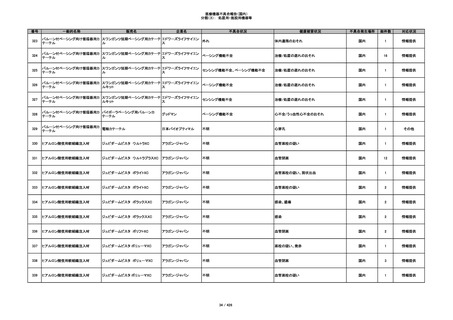
プラスチックカニューレ型滅菌済み穿刺
BD インサイト
針
日本ベクトン・ディッキンソ
切断
ン
体内遺残
国内
1
情報提供
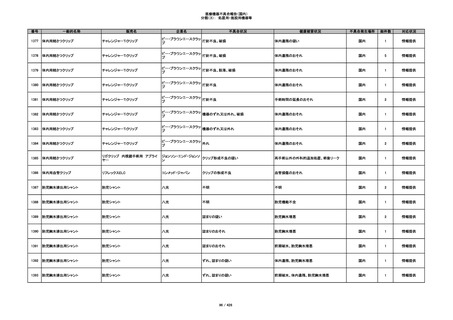
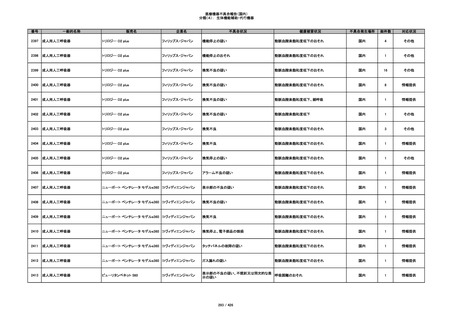
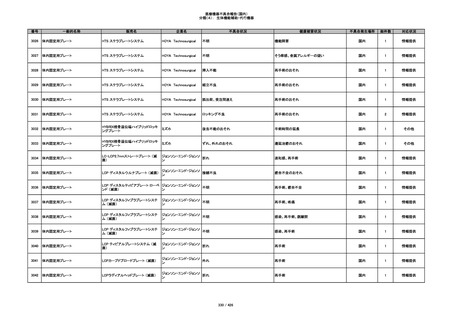
351
プラスチックカニューレ型滅菌済み穿刺
BD インサイト オートガード
針
日本ベクトン・ディッキンソ
収納困難
ン
感染のおそれ
国内
2
その他
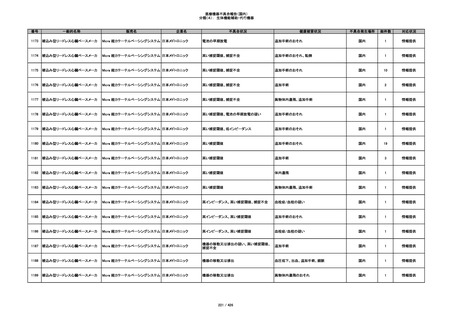
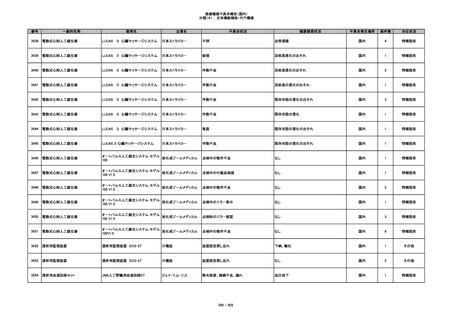
352
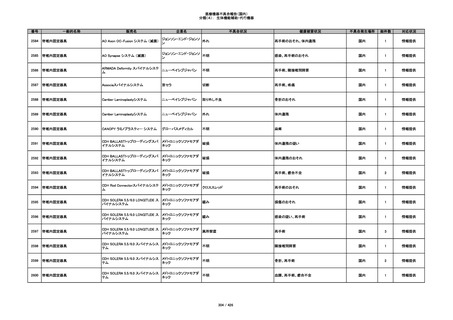
プラスチックカニューレ型滅菌済み穿刺
BD インサイト オートガード
針
日本ベクトン・ディッキンソ
収納困難
ン
感染のおそれ
国内
19
情報提供
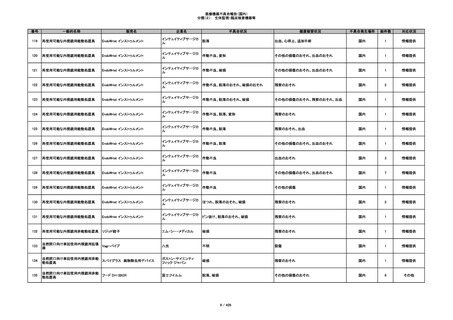
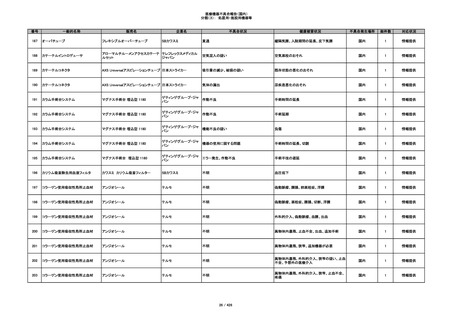
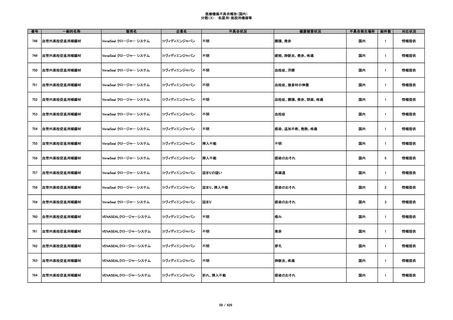
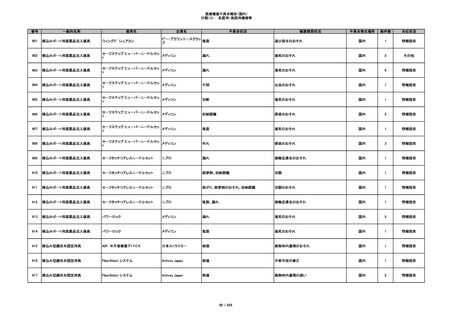
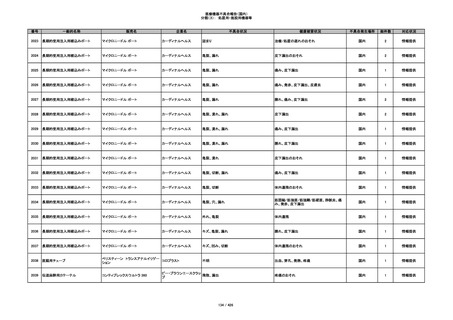
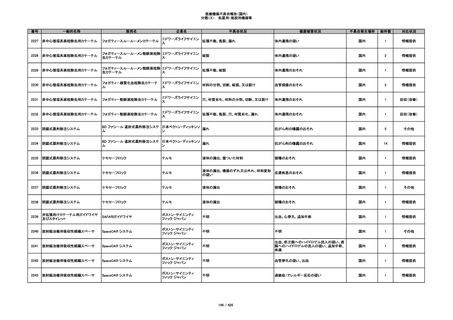
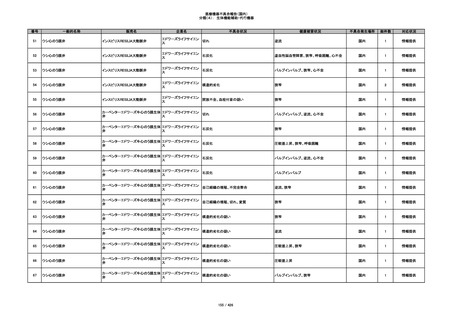
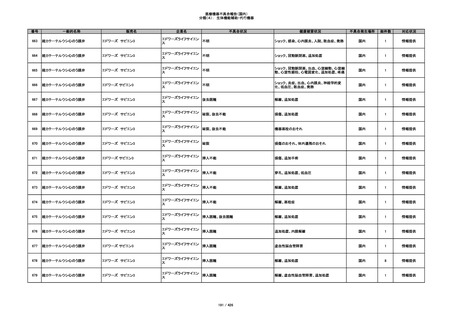
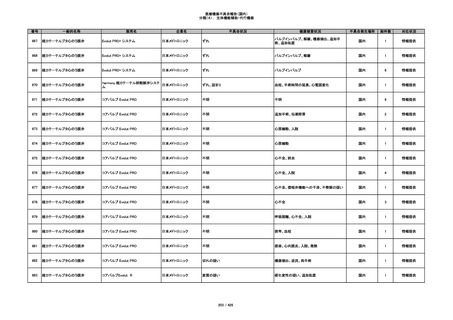
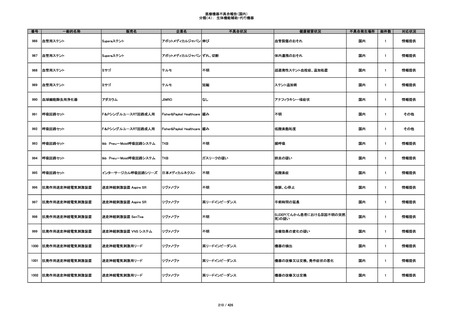
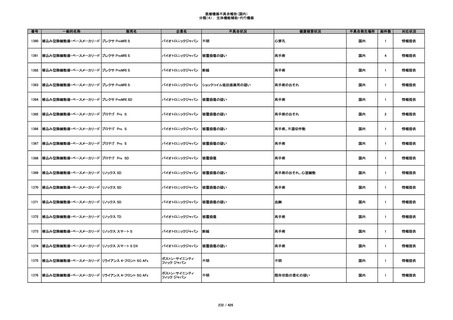
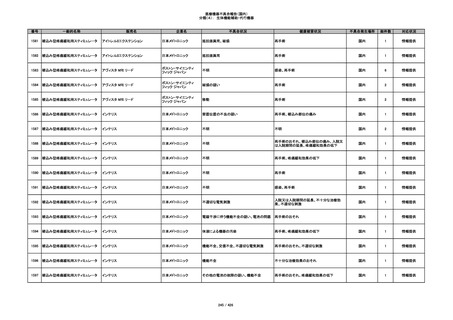
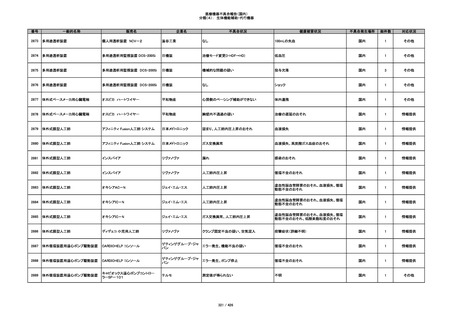
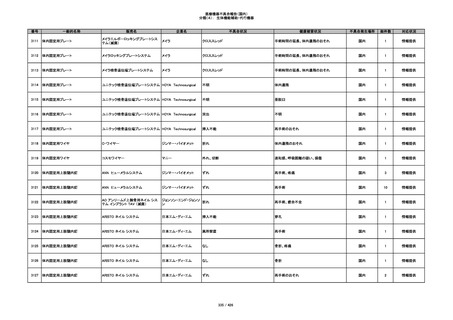
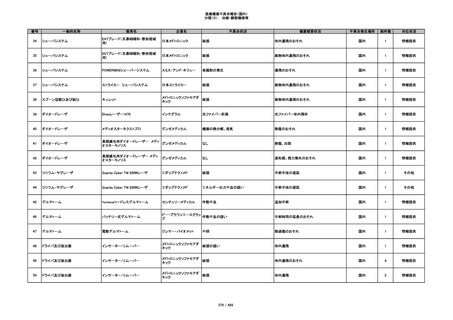
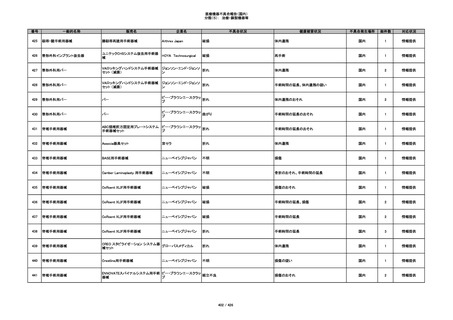
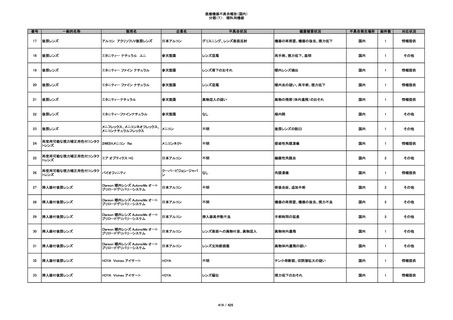
353
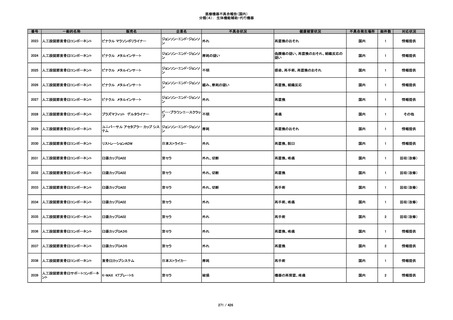
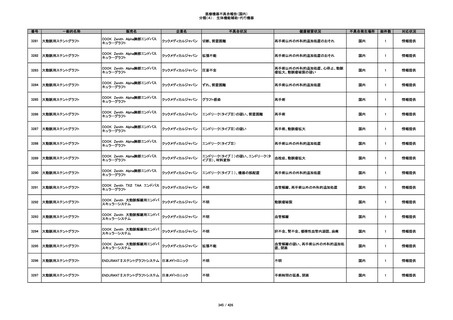
プラスチックカニューレ型滅菌済み穿刺
BD ネクシーバ
針
日本ベクトン・ディッキンソ
漏れの疑い
ン
抗がん剤の曝露のおそれ
国内
1
情報提供
354
プラスチックカニューレ型滅菌済み穿刺
BD ネクシーバ
針
日本ベクトン・ディッキンソ
収納困難
ン
感染のおそれ
国内
1
情報提供
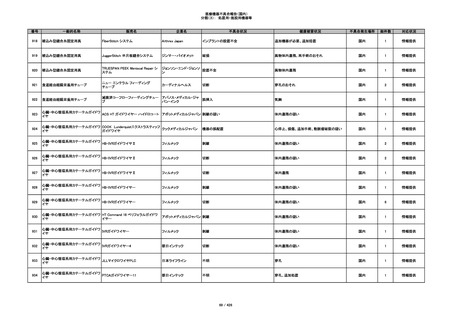
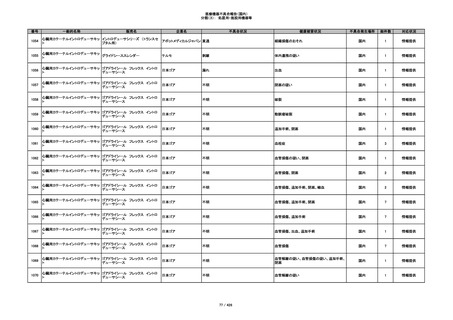
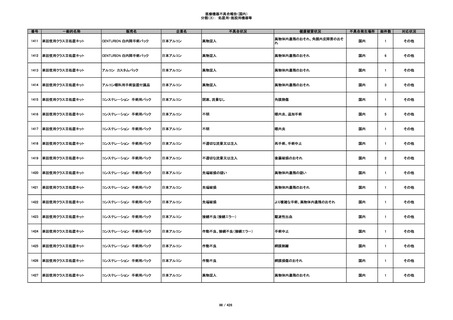
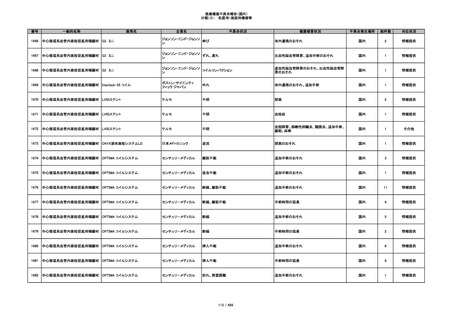
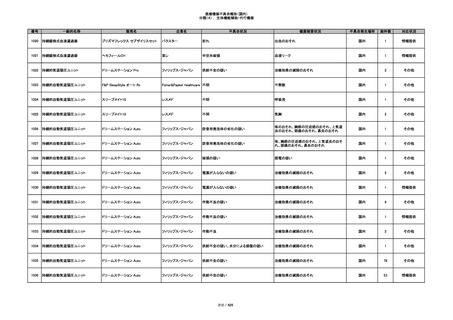
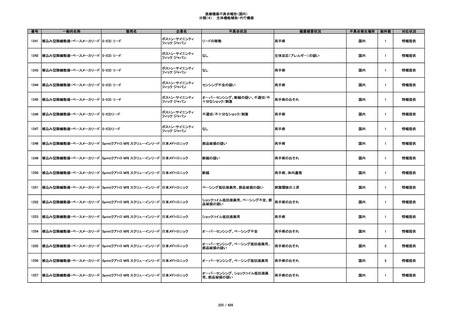
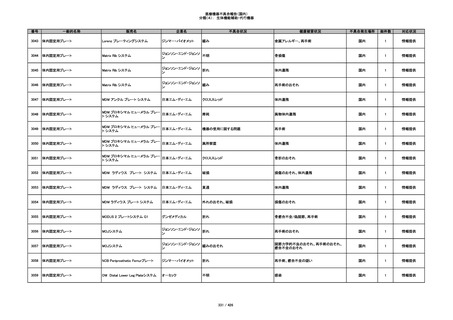
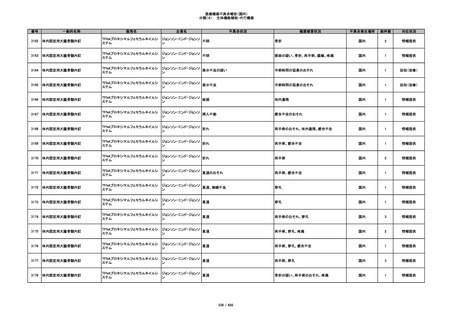
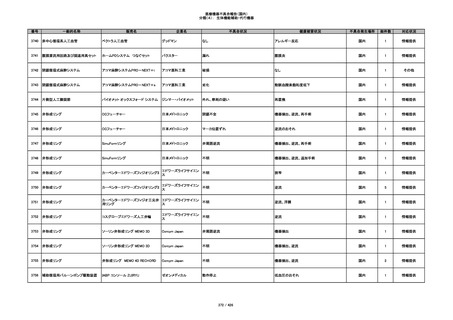
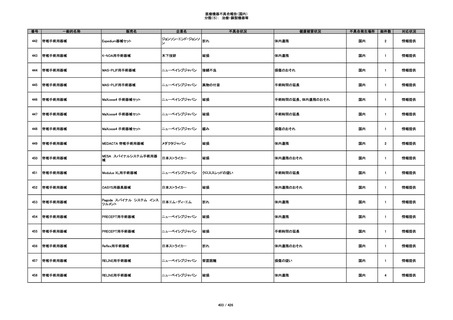
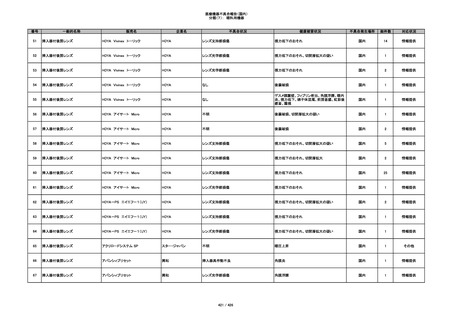
355
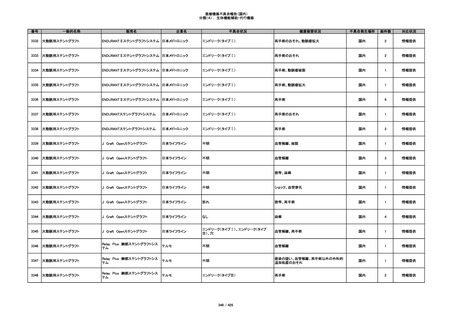
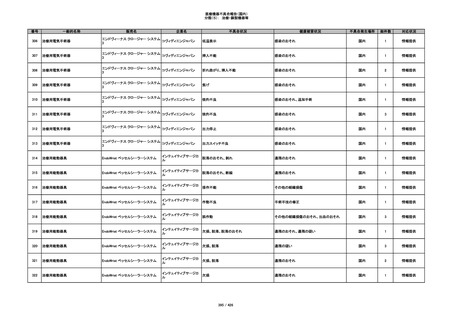
プラスチックカニューレ型滅菌済み穿刺
イントロカン セーフティ
針
ビー・ブラウンエースクラッ
漏れ
プ
過少投与のおそれ
国内
1
その他
356
プラスチックカニューレ型滅菌済み穿刺
イントロカン セーフティ
針
ビー・ブラウンエースクラッ
収納困難の疑い
プ
針刺し/穿刺のおそれ
国内
1
その他
35 / 426