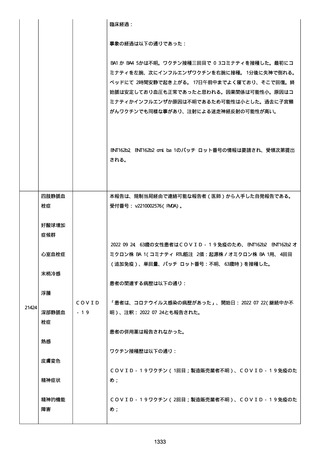
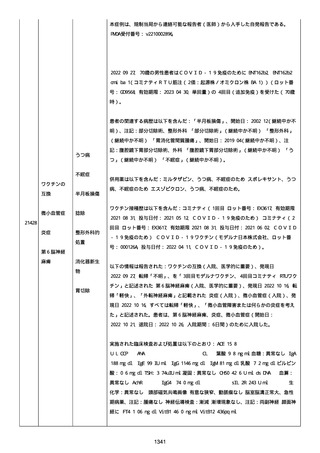
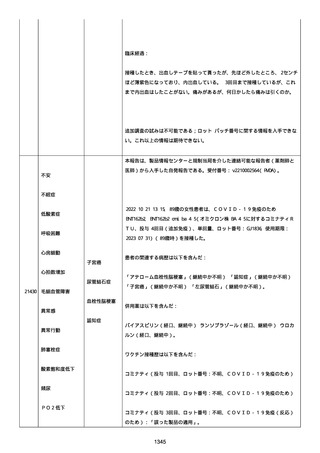
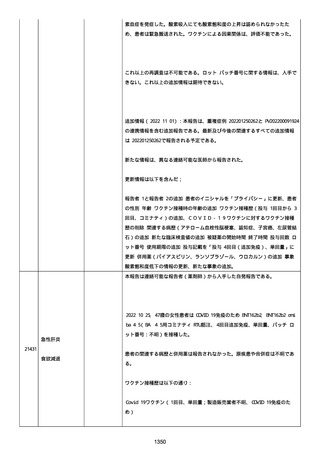
資料1-2-3-1 薬機法に基づく製造販売業者からの副反応疑い報告状況について(コミナティ筋注・集計対象期間における基礎疾患等及び症例経過) (1065 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00056.html |
| 出典情報 | 第89回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第21回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)(12/16)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
後に増悪した Basedow 病の 1 例」、The 23rd Chugoku Regional
Meeting of the Japan Endocrine Society、2022; Vol:23rd,
pgs:22。
48 歳の男性患者は covid-19 免疫のため投与回数不明の BNT162b2(コ
ミナティ、単回量、バッチ/ロット番号:不明)を接種した。
患者の関連病歴は以下を含んだ:
「バセドウ病」(継続中)。
併用薬は以下を含んだ:
MMI 服用(バセドウ病のため)。
以下の情報が報告された:
バセドウ病;
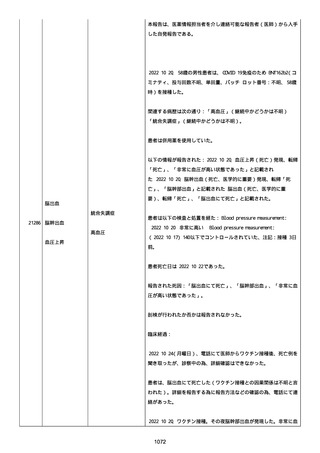
21282
バセドウ病
状態悪化
バセドウ病(入院、医学的に重要)、状態悪化(入院、医学的に重
要)、転帰「軽快」、全て「バセドウ病増悪/バセドウ病の増悪」と
記載された。
事象「バセドウ病増悪/バセドウ病の増悪」は診療所受診を必要とし
た。
患者は以下の臨床検査と処置を受けた:
抗甲状腺抗体:471 %、特記:上昇;
抗甲状腺抗体:12.6 IU/l、特記:上昇;
自己抗体:陽性;
血中甲状腺刺激ホルモン:検出可能な感知以下;
BMI:22、特記:kg/m2;
心臓超音波:EF 71%とやや過収縮、特記:心不全徴候なく;
EF:71 %;
1065