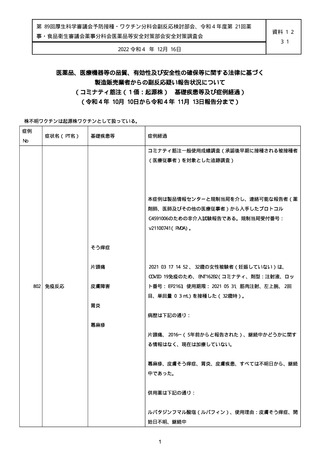
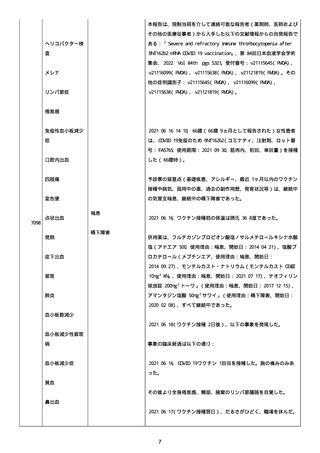
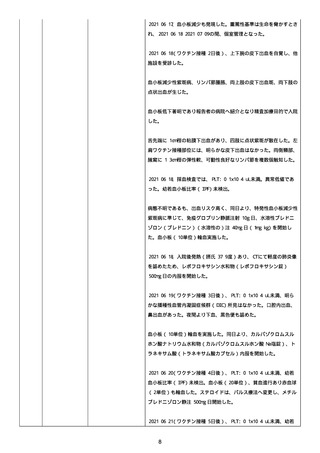
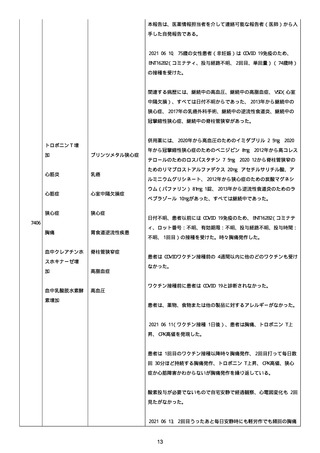
資料1-2-3-1 薬機法に基づく製造販売業者からの副反応疑い報告状況について(コミナティ筋注・集計対象期間における基礎疾患等及び症例経過) (1341 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00056.html |
| 出典情報 | 第89回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第21回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)(12/16)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
PMDA 受付番号:v2210002896。
2022/09/27、70 歳の男性患者はCOVID−19免疫のために BNT162b2、BNT162b2
omi ba.1(コミナティRTU筋注(2 価:起源株/オミクロン株 BA.1))(ロット番
号:GD9568、有効期限:2023/04/30、単回量)の 4 回目(追加免疫)を受けた(70 歳
時)。
患者の関連する病歴は以下を含んだ:「半月板損傷」、開始日:2002/12(継続中か不
明)、注記:部分切除術、整形外科;「部分切除術」(継続中か不明);「整形外科」
(継続中か不明);「胃消化管間質腫瘍」、開始日:2019/04(継続中か不明)、注
うつ病;
記:腹腔鏡下胃部分切除術、外科;「腹腔鏡下胃部分切除術」(継続中か不明);「う
つ」(継続中か不明);「不眠症」(継続中か不明)。
不眠症;
併用薬は以下を含んだ:ミルタザピン、うつ病、不眠症のため;スボレキサント、うつ
ワクチンの
互換;
半月板損傷;
微小血管症;
捻除;
炎症;
整形外科的
21428
処置;
第6脳神経
麻痺
消化器新生
物;
病、不眠症のため;エスゾピクロン、うつ病、不眠症のため。
ワクチン接種歴は以下を含んだ:コミナティ(1 回目;ロット番号:EX3617、有効期限
2021/08/31、投与日付:2021/05/12、COVID−19免疫のため);コミナティ(2
回目;ロット番号:EX3617、有効期限 2021/08/31、投与日付:2021/06/02、COVID
−19免疫のため);COVID−19ワクチン(モデルナ日本株式会社、ロット番
号:000126A、投与日付:2022/04/11、COVID−19免疫のため)。
以下の情報は報告された:ワクチンの互換(入院、医学的に重要)、発現日
2022/09/27、転帰「不明」、を「3 回目モデルナワクチン、4 回目コミナティ RTU ワク
胃切除
チン」と記述された;第6脳神経麻痺(入院、医学的に重要)、発現日 2022/10/16、転
帰「軽快」、「外転神経麻痺」と記載された;炎症(入院)、微小血管症(入院)、発
現日 2022/10/16、すべては転帰「軽快」、「微小血管障害または何らかの炎症を考え
た」と記述された。患者は、第6脳神経麻痺、炎症、微小血管症(開始日:
2022/10/21、退院日:2022/10/26、入院期間:6 日間)のために入院した。
実施された臨床検査および処置は以下のとおり:ACE 15.8
U/L;CCP(-);ANA(-);(-);(-);(-);(-);(-);CL(-);葉酸 9.8 ng/ml;血糖:異常なし;IgA
188 mg/dl ;IgE 99 IU/ml ;IgG 1146 mg/dl ;IgM 81 mg/dl;乳酸 7.2 mg/dl;ピルビン
酸:0.6 mg/dl;TSH:3.74uIU/ml;凝固:異常なし;CH50 42.6 U/ml;ds-DNA(-);血算:
異常なし;AchR(-);(-);IgG4: 74.0 mg/dl;(-);(-);(-);sIL-2R 243 U/ml;(-);(-);生
化学:異常なし; 頭部磁気共鳴画像:有意な狭窄、動脈瘤なし;脳室脳溝正常大、急性
期病巣、注記:腫瘍なし;神経伝導検査:漸減
·
漸
増
現
象
な
し
、
注
記
:
両
副
神
経
,顔面神
経に;FT4 1.06 ng/dl;VitB1 46.0 ng/ml;VitB12 436pq/ml.
1341