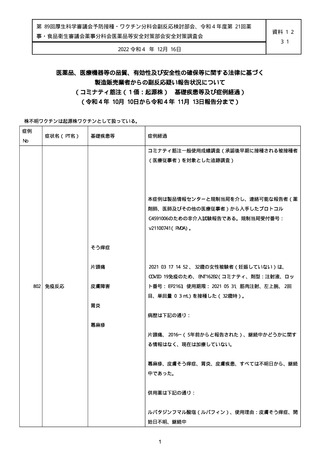
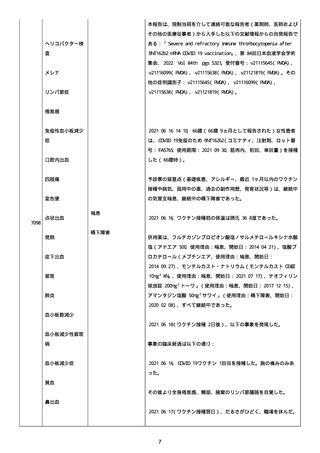
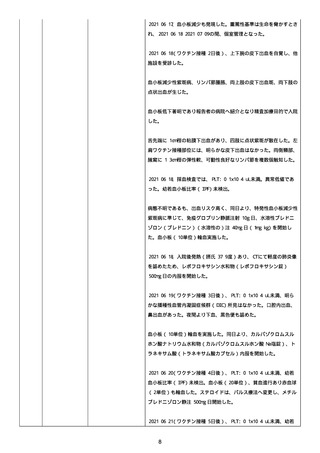
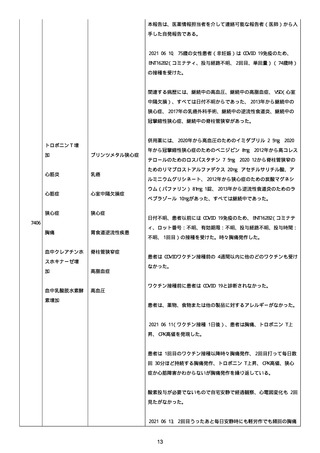
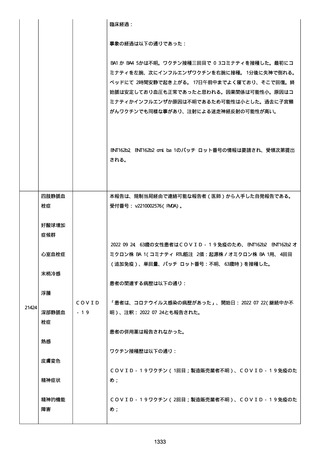
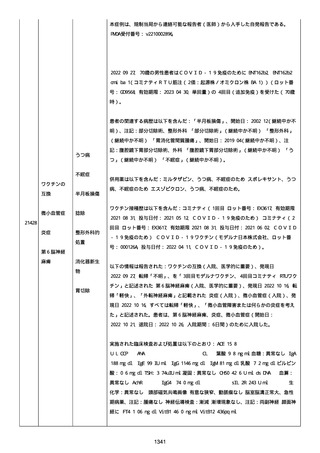
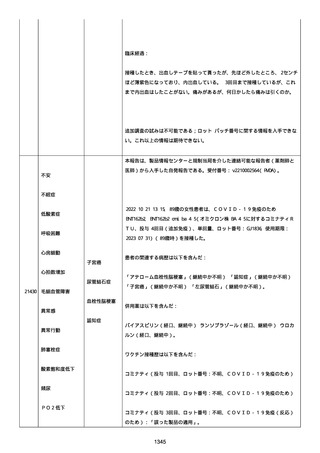
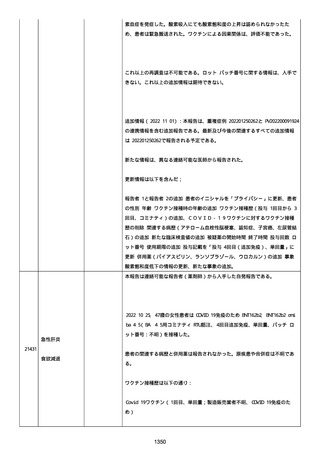
資料1-2-3-1 薬機法に基づく製造販売業者からの副反応疑い報告状況について(コミナティ筋注・集計対象期間における基礎疾患等及び症例経過) (250 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00056.html |
| 出典情報 | 第89回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第21回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)(12/16)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
最終的範囲は、報告されたロット番号 EP2163 に関連していると決定
された。苦情サンプルは返却されなかった。
関連する品質問題は調査中に特定されなかった。
製品の品質、規制、バリデーションおよび安定性への影響はなかっ
た。
製造所は、報告された欠陥が、バッチ全体の品質の典型的なものでは
なく、バッチは引き続き適合であると結論した。
NTM プロセスは、規制当局への通知は不要と判断した。
報告された欠陥は調査により確認することができなかった。
苦情が確認されなかったため、根本原因または CAPA も特定されなか
った。
報告者意見:
事象は BNT162b2 と関連はなかった。
追加情報(2022/06/20):
本報告は、プロトコル C4591006 に関する非介入試験の追加報告であ
る。
更新された情報は以下の通り:
被験者情報(身長、体重、人種)、病歴、臨床検査値、事象因果関
係、報告者意見。
追加情報(2022/06/28):
250