資料1-2-3-1 薬機法に基づく製造販売業者からの副反応疑い報告状況について(コミナティ筋注・集計対象期間における基礎疾患等及び症例経過) (795 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00056.html |
| 出典情報 | 第89回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第21回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)(12/16)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
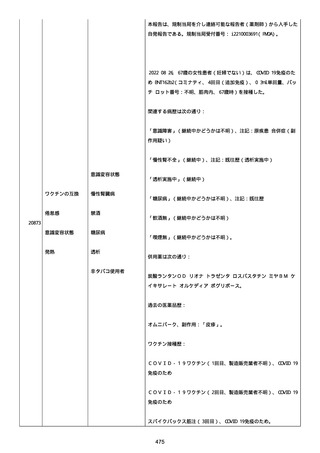
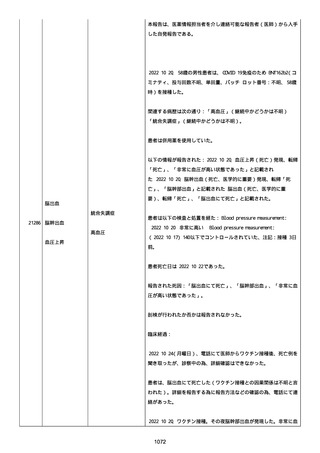
ンの初回接種を受け、2 回目の投与を 2021 年 8 月 3 週目に受けた。
2021 年 9 月 1 週目に、患者は、発熱と全身疲労感を発現した。
SARS-CoV-2 逆転写ポリメラーゼ連鎖反応(RT-PCR)(鼻スワブ)検
査は陽性であり、患者は回復施設にとどまった。
2021 年 9 月中旬、SARS-CoV-2RT-PCR 検査は陰性で、患者は施設から
退院した。
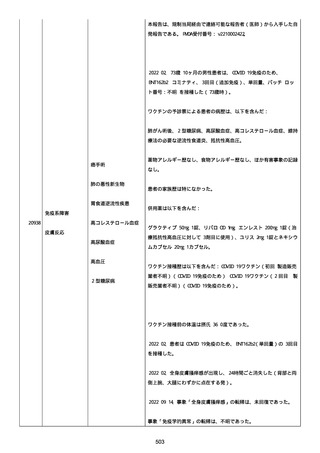
その後、患者は発熱、進行性労作性呼吸困難を発現し、2021 年 9 月
下旬、肺炎の治療のため病院に入院した。
患者の体温は 38.6 度、経皮的酸素飽和度(SpO2)は室内気で 92%で
あった。
胸部コンピューター断層撮影(CT)は、両肺に多発性非区域性硬化像
を認めた。
血液検査では、血清C−反応性蛋白(CRP)値上昇と低γグロブリン
血症を認めた。
入院時、鼻咽頭 SARS-CoV-2PCR スワブは陰性であった。
患者は、市中感染性肺炎のため、アジスロマイシンとセフトリアキソ
ンによる経験的抗菌薬療法を開始した。
咽頭マイコプラズマ抗原、血清クリプトコックス抗原と尿肺炎球菌抗
原検査は全て陰性であった。
4 日目、入院時に MCD の再発が特定されたため、患者のプレドニゾロ
ン用量は 15mg/日に増量された。
7 日目、喀痰培養で MSSA が確認され、メチシリン感受性黄色ブドウ
球菌(MSSA)肺炎のため、セフトリアキソンからセファゾリンへ切り
替えた。
8 日目、患者は、発熱と低酸素血症を伴う進行性呼吸困難を発現し
た。
SpO2 は、6L/分の酸素流量によるマスク下で 95%であった。
795