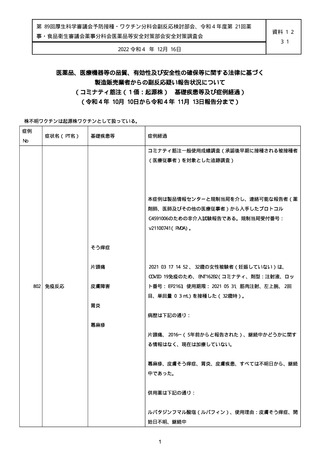
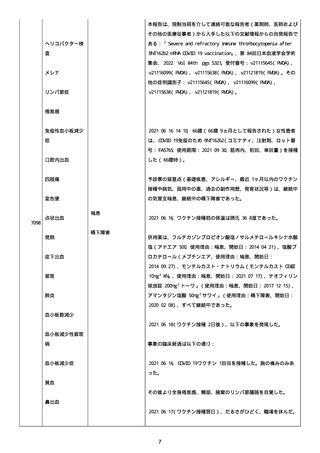
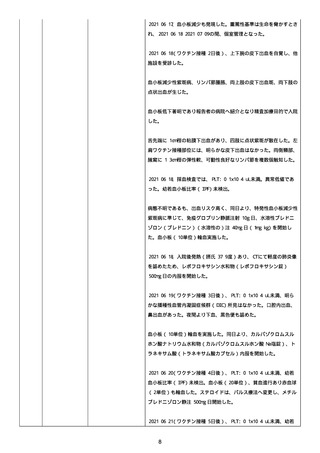
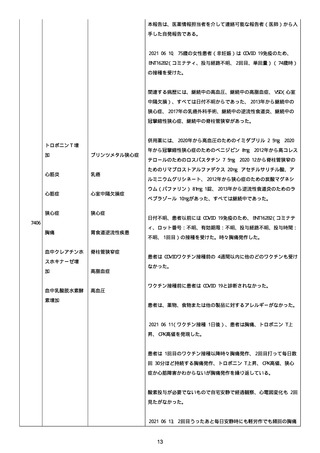
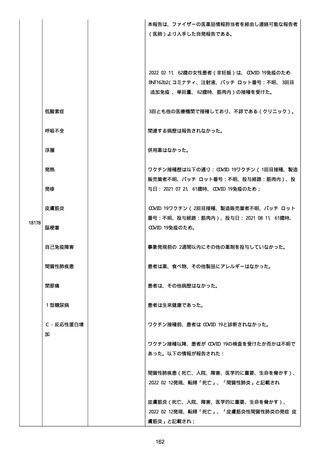
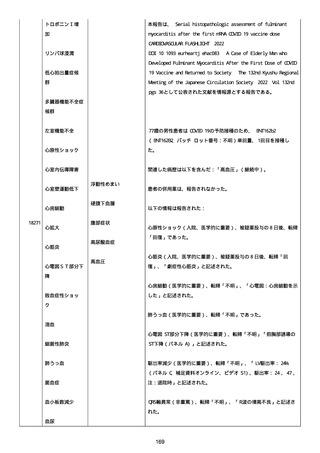
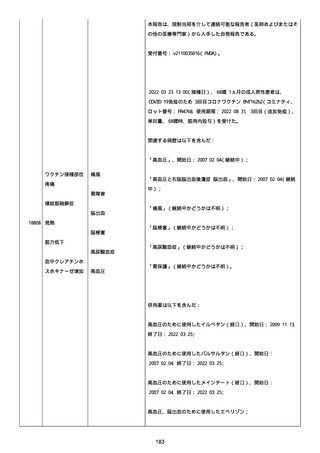
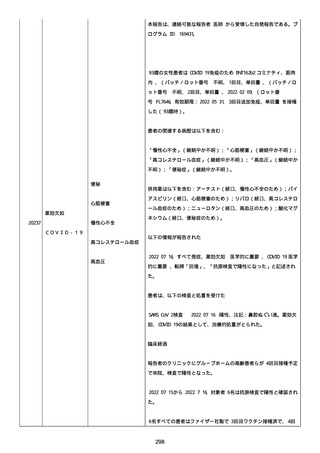
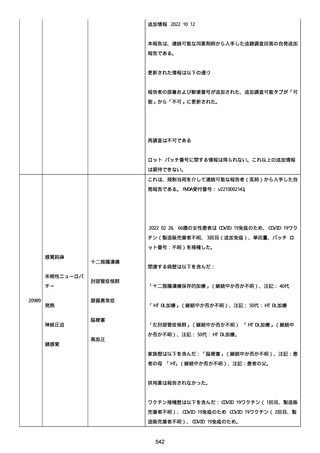
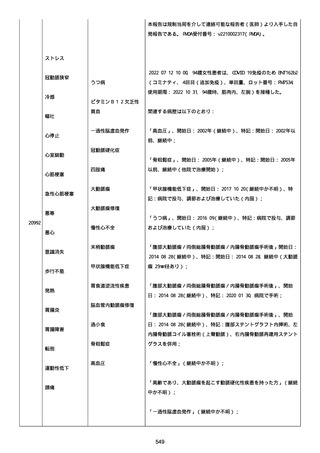
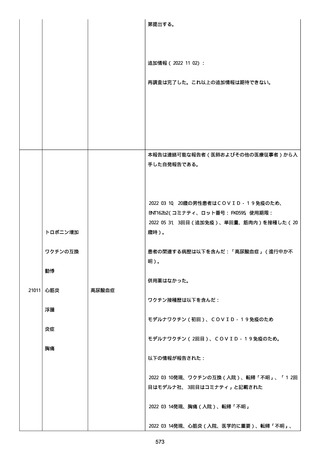
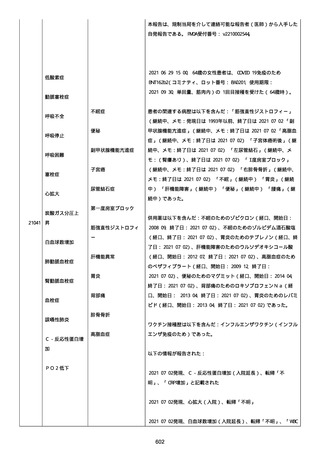
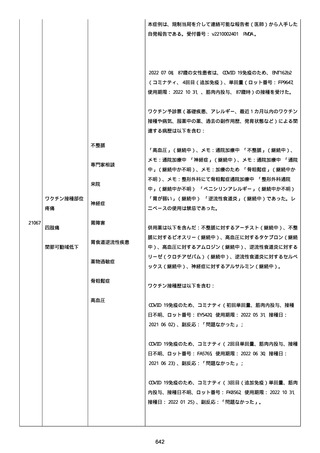
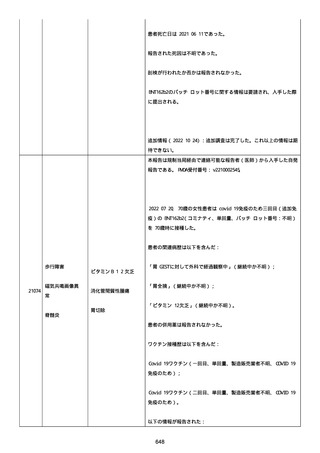
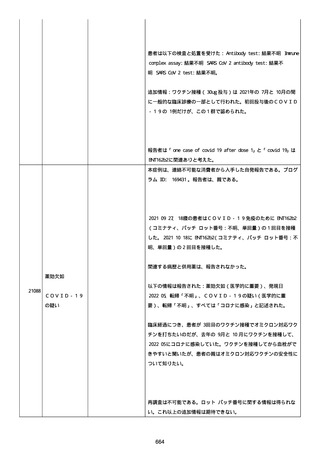
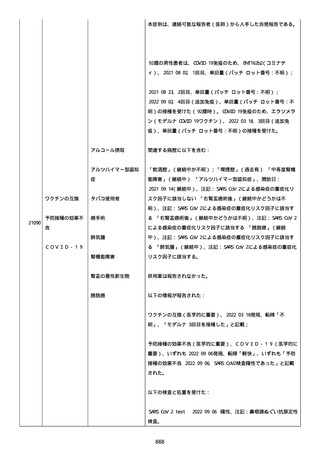
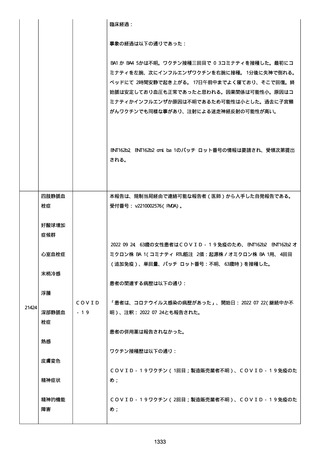
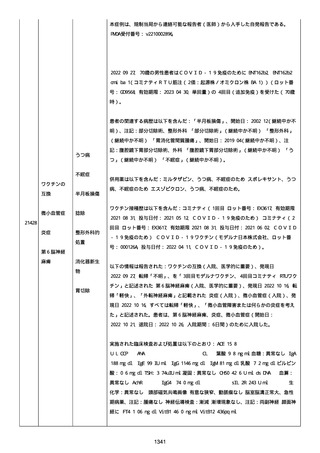
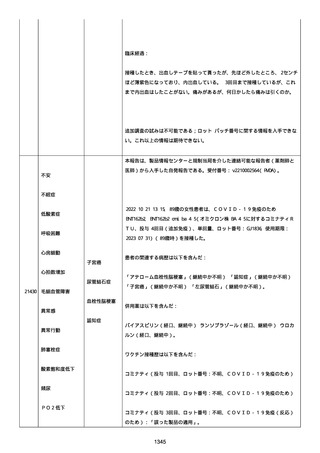
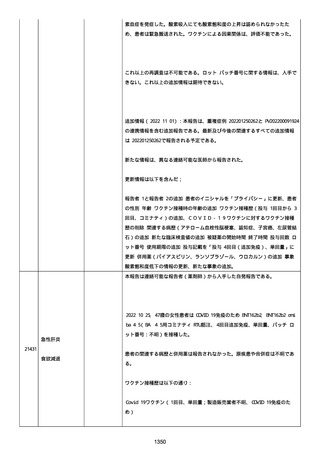
資料1-2-3-1 薬機法に基づく製造販売業者からの副反応疑い報告状況について(コミナティ筋注・集計対象期間における基礎疾患等及び症例経過) (973 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00056.html |
| 出典情報 | 第89回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第21回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)(12/16)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
CT:(2022 年)明らかな腫瘍は認められず;
直接 Coombs 試験:(2022 年)陽性;
サイトメガロウイルス検査:(2022 年)陰性;
上部消化管内視鏡:(2022 年)出血は認められなかった;
EBV 抗体:(2022 年)陰性;
Hct:(2022 年)24.6 %;
Hb:(2022 年)8.2 g/dl;(2022 年)11.1 g/dl;
ハプトグロビン:(2022 年)低下;
HIV 抗体:(2022 年)陰性;
MCV:(2022 年)100.8 fl;
マイコプラズマ検査:(2022 年)陰性;
赤血球数:(2022 年)結果不明;
網状赤血球:(2022 年)上昇;
リウマトイド因子:(2022 年)陰性;
血清フェリチン:(2022 年)正常範囲;
ウイルス検査:(2022 年)陰性。
治療処置は末梢性ニューロパチー、四肢痛の結果として実施された。
臨床情報:
3 回目としてファイザーワクチンを接種した。
973