資料1-2-3-1 薬機法に基づく製造販売業者からの副反応疑い報告状況について(コミナティ筋注・集計対象期間における基礎疾患等及び症例経過) (82 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00056.html |
| 出典情報 | 第89回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第21回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)(12/16)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
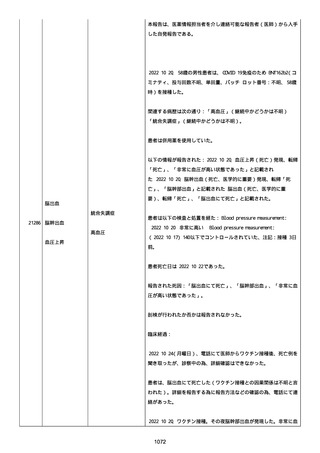
く、救急要請された。
救急接触時、脈なく心肺蘇生開始された。
心室細動(Vf)確認され、6 回直流除細動器(DC)施行し、心肺再開
を得て当院へ搬送された。
心臓カテーテル検査施行されたが、有意狭窄はなかった。
造影結果より、何かしらの要因による心筋症由来の心室細動が疑われ
た。
頭部 MRI よりクモ膜下嚢胞確認され、一時的な心肺停止に起因してい
る可能性否定できない。
2021/09/22、臨床検査として COVID-19 PCR 検査を実施し、結果は陰
性であった。
2021/09/22 の臨床検査は血液検査と生化学的検査を含み、結果は提
供されなかった。
2021/10/05、心臓ペースメーカーの植込みが実施された。
患者は、心血管系の多臓器障害があった:意識消失、Vf 確認にて、
DC 6 回施行された。
その他の症状/徴候:クモ膜下嚢胞が確認され、一時的な心肺停止に
起因している可能性否定できない。
報告薬剤師は事象を重篤(入院)と分類し、事象と BNT162B2 との関
連ありと評価した。
他の要因(他の疾患など)の可能性はなかった。
報告された心筋症は劇症型ではなかった。
報告者意見:
82